脳深部の光操作を可能にするために開発
東京大学物性研究所は5月10日、ロドプシンのアミノ酸を改変することで、従来よりも長波長の光で操作が可能な新しい人工ロドプシンタンパク質を作製することに成功したと発表した。この研究は、東京大学物性研究所の井上圭一准教授と名古屋工業大学大学院工学研究科 生命・応用化学専攻の神取秀樹教授らはイタリアのシエナ大学などとの国際共同研究によるもの。研究成果は、英国のオンライン科学雑誌「Nature Communications」誌に4月30日付で掲載された。
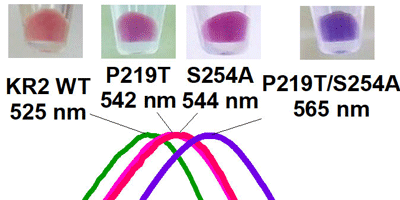
画像はリリースより
ヒトを含む動物は、目の中の網膜にある細胞を使って光をとらえ、物体の形や色を認識する。その際に、光を吸収し脳に視覚情報を伝える役割を持つのが「ロドプシン」と呼ばれるタンパク質。近年、遺伝子操作技術を用いて、マウスやゼブラフィッシュなどの動物の脳神経ネットワークを構成する特定の神経細胞に微生物型のロドプシンを導入し、ロドプシンが行うイオン輸送を通じて、神経細胞の興奮や抑制を光で自在に操作するオプトジェネティクス(光遺伝学)技術が注目を集めている。
この技術を用いることで、脳神経ネットワーク内の神経細胞のつながりや、さまざまな種類の神経細胞が関わる行動や感情、思考、精神疾患などについて調べることができる。しかし、脳などの生体組織は光を強く散乱する性質を持つことから、青や緑色などの従来のロドプシンの動作に必要とされていた比較的短波長の光では、脳深部の光操作が困難だった。そのため、より長波長の光である黄色や赤色の光で操作可能なロドプシンの開発が望まれていた。
アミノ酸変異で吸収波長の長波長化に成功
今回研究グループは、すべてのロドプシンに存在している、光を受け取る役割を持つ「レチナール」に注目。レチナールを取り囲むアミノ酸のパターンは、タンパク質ごとに異なり、それによって吸収波長が決められている。そこで研究グループは、Na+を輸送するNa+ポンプ型ロドプシンの、レチナール近傍にあるアミノ酸の化学的性質を変えることで、レチナールの持つ電子の状態を制御し、より長波長の光を吸収する分子のデザインを試みた。
その結果、野生型のNa+ポンプ型ロドプシンより40nmも長波長の光で駆動する、これまでにない分子の作製に成功した。吸収波長が大きく変化しているにも関わらず、イオンの輸送能は野生型のNa+ポンプと同等であり、極めて性能のよい分子ツールであることが示された。また、赤外分光法や計算機シミュレーションにより、作製した長波長吸収型のNa+ポンプ型ロドプシンの分子構造と長波長吸収化のメカニズムも明らかとなった。さらに、今回発見された「変異によるレチナールの吸収波長の変化」は、自然界に存在する特定の細菌の中でも生じていることがわかり、自然界で起こるタンパク質の進化についても新たな知見が得られたという。
今回の成果により見出された、アミノ酸変異による吸収波長の長波長化は、Na+ポンプ型ロドプシン以外の数多くのロドプシンに適用が可能。同技術を用いて今後さらに優れた分子ツールの開発と、それを用いたオプトジェネティクスによる脳科学研究の進展が期待されると研究グループは述べている。
▼関連リンク
・東京大学 物性研究所 プレスリリース




