IFNによる治療効果が低い、2型糖尿病のC型肝炎患者
金沢大学は4月11日、C型肝炎ウイルス(HCV)感染時に、主に肝臓で産生される分泌タンパク質であるセレノプロテインPのmRNAが、抗ウイルス免疫分子であるRIG-I(Retinoic acid-inducible gene-I)と結合することで、その機能を阻害し、自然免疫機構を制御することを明らかにしたと発表した。この研究は、金沢大学医薬保健研究域保健学系の本多政夫教授および村居和寿博士研究員らの研究グループが、同医薬保健研究域医学系の金子周一教授および篁俊成教授らとともに行ったもの。研究成果は、米国科学誌「Cell Host & Microbe」のオンライン版に4月10日付で掲載された。
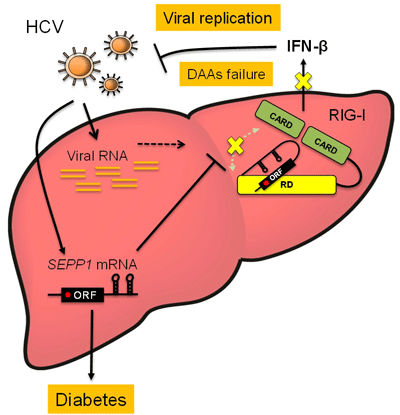
画像はリリースより
C型肝炎に感染すると、同時に、2型糖尿病になりやすいことが知られている。また、C型肝炎の治療には抗ウイルス薬の投与などを使用する治療が中心となるが、2型糖尿病を患ったC型肝炎患者では、インターフェロン(IFN)による抗ウイルス治療の効果が低いことが報告されていた。しかし、そのメカニズムや因果関係は未だ明らかにはされていなかった。
同研究グループは以前、肝臓由来の分泌タンパクであるセレノプロテインPがインスリン抵抗性を引き起こし、2型糖尿病の病態形成に関与することを世界に先駆けて報告した。興味深いことに、2型糖尿病を併発したC型慢性肝炎患者においては、IFNによる抗ウイルス治療に対し抵抗性を示す傾向があると報告されている。そこで今回の研究では、セレノプロテインPに焦点を当て、HCV感染と2型糖尿病の臨床的関連性を検討した。
セレノプロテインP高発現で抗ウイルス治療が効きにくくなると判明
まず、セレノプロテインPが肝臓での抗ウイルス免疫応答に与える影響を検討した。その結果、HCV感染は培養細胞でセレノプロテインPの発現を上昇させることがわかった。また、健常人と比べてC型慢性肝炎患者では血清中のセレノプロテインPの発現が上昇しているとともに、セレノプロテインPが高発現している患者群においては、DAAs(Direct-acting antiviral drugs)を用いた抗ウイルス治療が効きにくいことが明らかとなった。
一方、セレノプロテインPの発現を抑制した細胞では、HCV複製が顕著に抑制され、抗ウイルス作用を有するIFNの産生が亢進していることが明らかになった。細胞内に侵入したウイルス由来の RNA を認識してIFN産出を誘導する代表的な分子として、RIG-I と MDA5が報告されている。両分子は、認識できるRNAの構造や配列(PAMP)が異なっているが、HCVは RIG-I と MDA5いずれにも認識され得ると考えられている。そこで、RIG-IとMDA5をノックアウトした細胞を用いて実験を行なったところ、セレノプロテインPはRIG-I経路に依存した自然免疫応答を特異的に制御していることが分かった。さらに詳細に検討した結果、セレノプロテインPによる自然免疫制御は、タンパク質ではなく、mRNAによって引き起こされることが明らかになった。
セレノプロテインPのmRNAがRIG1に結合して自然免疫を負に制御
RIG-IにウイルスRNAが結合すると、RIG-IのATPアーゼ活性が働いて立体構造の変化およびRIG-Iの多量体形成が起こり、ミトコンドリア膜上のタンパク質と結合することでIFN産生シグナルが活性化する。セレノプロテインPのmRNAを過剰発現させたところ、RIG-IのATPアーゼ活性、RIG-Iの多量体形成、ミトコンドリアへの局在が阻害されることが分かった。その制御メカニズムとして、セレノプロテインPのmRNAは、RIG-Iの制御ドメインに特異的に結合して相互作用することにより、RIG-Iの活性化に必要な立体構造変化を阻害し、自然免疫を負に制御していることが明らかとなった。
また、290例のC型肝炎患者にダクラタスビルとアスナプレビルのDAAs療法を行った治療成績から、治療不成功例では、治療前のウイルスの薬剤耐性変異の存在と共に、血中のセレノプロテインPの値が高いことが明らかになり、2型糖尿病を併発したC型慢性肝炎患者では、DAAs療法が効きにくくなる可能性が示唆された。
以上のことから、肝臓における抗ウイルス免疫制御機構の1つとして、セレノプロテインPのmRNAによるRIG-Iを介した自然免疫の制御機構が明らかとなった。本来、RIG-Iは、自分自身のRNAには作用しないと知られていた。今回の研究によって得られた知見は、肝臓における免疫寛容や自己免疫疾患の理解に重要な情報を提供すると考えられ、また、RIG-Iを制御する自己RNAの研究に拍車がかかり、そのmRNAを治療標的とした核酸医薬への応用にも期待できると研究グループは述べている。
▼関連リンク
・金沢大学 研究トピック




