白血病発症の新たな分子メカニズムを探る
日本医療研究開発機構(AMED)と大阪大学は3月6日、リボヌクレアーゼであるRegnase-1が造血幹細胞および造血前駆細胞の自己複製を制御していることを明らかにし、また、Regnase-1遺伝子を欠失させたマウスでは急性骨髄性白血病と類似した症状を示すことを発見したことにより、Regnase-1が白血病の発症に関与していることを明らかにしたと発表した。この研究は、大阪大学微生物病研究所の木戸屋浩康助教、高倉伸幸教授(免疫学フロンティア研究センター兼任)らの研究グループによるもの。研究成果は日本時間の同日、「Nature Communications」(オンライン)に掲載された。
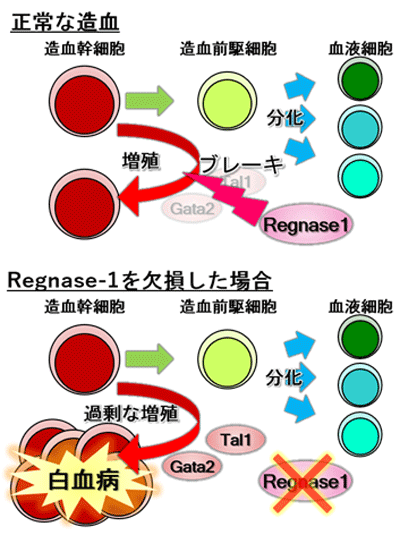
画像はリリースより
血液の幹細胞である造血幹細胞や造血前駆細胞の増殖や分化が異常になると、白血病の発症につながる。そうした異常が起きないように、造血幹細胞はさまざまな分子によって緻密に増殖と分化のバランスが制御されているが、今回研究グループが着目した「Regnase-1」も、造血幹細胞の異常な増殖に対するブレーキとして働く分子のひとつ。Regnase-1は標的とする特定のRNAを分解する働きを持つ分子(リボヌクレアーゼ)で、遺伝子の発現量を制御する役割を持つことは既に報告されていた。
リボヌクレアーゼ「Regnase-1」の異常が白血病発症に関与
今回研究グループは、Regnase-1遺伝子を欠失したマウスを用いて、白血病発症との関連性を解析した。造血幹細胞の増殖や分化の制御は生命活動の維持に重要であり、異常が起きないように点検機構が働いているため、単一の遺伝子異常が起きても白血病が発症することは稀だが、Regnase-1遺伝子を欠失したマウスはわずか3か月ほどで重篤な造血異常によって死亡する。その原因を調べるため、Regnase-1の機能を解析したところ、Regnase-1がGata2やTal1といった造血幹細胞の制御に重要な転写因子のmRNAを分解することで、造血幹細胞の増殖を制御する転写ネットワークを制御していることが判明。そのため、Regnase-1のみの欠失でも広範囲の遺伝子発現の変化が誘導されてしまい、白血病の発症が誘導されてしまうのだという。
今回の研究では、マウスモデルを用いた実験により、Regnase-1遺伝子を欠失した造血幹細胞が過剰に増殖し続け、白血病を発症することが明らかとなった。これまで、造血幹細胞制御や白血病発症に関わる遺伝子として、エピジェネティック制御やシグナル伝達制御分子などが見つかっていたが、今回の研究により、これまでに考えられてこなかったリボヌクレアーゼも関与していることが初めて明らかとなった。
白血病は若年層に多く発症するがんであり、同世代のがんの約4分の1とも言われている。治療法の発展によって寛解できるようになりつつあるが、患者の多くは再発の恐怖に悩まされており、完全寛解を可能とする治療法の開発が望まれている。今回、白血病の原因となる分子機構が新たに同定されたことで、Regnase-1などを標的とした新概念に基づく白血病治療薬や再発抑制薬の開発が期待される、と研究グループは述べている。
▼関連リンク
・日本医療研究開発機構 プレスリリース



