炎症性腸疾患などの原因・病態に関与する小胞体ストレス
大阪市立大学は3月1日、炎症性腸疾患の腸管上皮細胞の小胞体ストレスが、抗体のひとつである免疫グロブリンA(IgA)の産生を誘導することを明らかにしたと発表した。この研究は、同大大学院医学研究科 消化器内科学の細見周平講師らの研究グループによるもの。研究成果は学術誌「Science」に掲載されている。
画像はリリースより
小胞体ストレスとは、変性タンパク質が細胞内の小胞体へ蓄積した状態を指す。腸内細菌や食物抗原にさらされている腸管では、多くの粘液や抗菌ペプチドの産生が必要であることから、常に小胞体ストレス状態にある。この小胞体ストレスが過剰になると、細胞への悪いストレス(Distress)が生じ、結果、種々の疾患の原因・病態に関与することが知られている。
これまでの報告から、炎症性腸疾患と総称される潰瘍性大腸炎やクローン病では、腸管が過剰な小胞体ストレス状態にあることがわかっている。また、小胞体ストレス応答を制御する主要な転写因子であるX-box-binding protein 1(Xbp1)の機能低下型変異が、炎症性腸疾患の発症リスクとなる遺伝的背景として同定されている。これらを裏付けるように、Xbp1遺伝子を腸管上皮細胞で特異的に欠損させたマウスでは、過剰な小胞体ストレス状態が認められ、その結果、クローン病に類似した自然発症小腸炎が生じることも証明されている。しかし、腸管小胞体ストレスの粘膜保護的な作用、つまり腸管への良いストレス(Eustress)を検討した研究はなかった。
小腸粘膜IgAが増加しているヒトでも同様の結果に
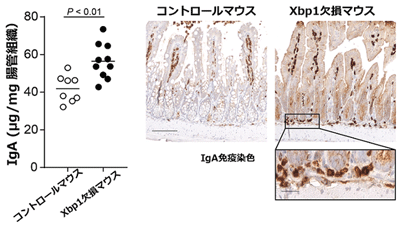
研究グループは、腸管上皮細胞特異的Xbp1欠損マウス(Xbp1欠損マウス)の詳細な解析を行った。その結果、過剰な腸管小胞体ストレス状態にあるマウスの腸管では、免疫グロブリンA(IgA)の産生が促進されていることが判明。また、IgAは小腸組織中だけでなく、血漿中や小腸の内腔でも濃度が上昇していることが判明した。
腸管粘膜面においては、病原体の感染への防御機能だけでなく、常在菌のバランス維持にもIgA抗体が重要な役割を担っていることが知られている。そこで、Xbp1欠損マウスに生じる自然発症小腸炎におけるIgAの役割を解明するため、IgAやB細胞(抗体産生細胞に分化する細胞)も同時に欠損したXbp1欠損マウスの解析を行ったところ、IgAがXbp1欠損マウスの小腸炎を抑える作用を有することが明らかとなった。つまり、腸管小胞体ストレスは、腸炎を導こうとするDistressを引き起こすと同時に、腸炎を抑えようとするEustressとしての一面も持っていることがわかった。
腸管IgAの産生には、T細胞依存性とT細胞非依存性の2つの誘導経路が知られている。T細胞依存性経路は、主に小腸パイエル板とよばれる二次リンパ器官で抗原特異的にIgAが誘導される。一方、T細胞非依存性経路については、樹状細胞から産生される分子によって誘導される経路や、B細胞の一種であるB1細胞から誘導される経路などが報告されているが、未だ解明されていない点が多い経路だ。そこで、T細胞やパイエル板も同時に欠損したXbp1欠損マウスを解析したところ、小胞体ストレスで誘導されるIgAはT細胞非依存性に誘導されることが明らかになった。また、無菌マウスの検討から、炎症や腸内細菌叢にも依存しないことが判明。Xbp1欠損マウスの腹腔内においてはIgA産生B1b細胞(B1細胞の一つ)が増加していることがわかり、腹腔内B1b細胞が腸管小胞体ストレスによるIgA誘導の経路であることが判明した。さらに、腸管小胞体ストレスの増加が生じる遺伝子背景を持つヒト(ATG16L1T300A)において、小腸粘膜IgAが増加していたことから、人間でも同様に生じていることが明らかとなった。
今回の研究成果から、腸管小胞体ストレスがT細胞非依存性にIgA産生を誘導し、腸管の炎症を抑える作用をもつことが判明した。この発見は、腸管の恒常性維持機構を理解する上で重要であると考えられる。研究グループは、「このメカニズムは、腸管小胞体ストレスによる炎症に対する腸管恒常性維持機構として重要な働きであり、炎症性腸疾患の病因解明を紐解く成果と考えられる」と、述べている。
▼関連リンク
・大阪市立大学 新着情報



