骨細胞が発現する骨保護因子「Sema3A」に着目
東京医科歯科大学は1月15日、閉経後骨粗しょう症や加齢での骨量減少の原因が、骨細胞での Sema3A発現低下によることを突き止めたと発表した。この研究は、同大大学院医歯学総合研究科分子情報伝達学分野の中島友紀教授と林幹人助教らの研究グループが、東京大学大学院医学系研究科免疫学分野の高柳広教授、同研究科骨免疫学寄付講座、同研究科整形外科学分野の田中栄教授、同研究科ロコモ予防学寄付講座の研究グループと共同で行ったもの。研究成果は、国際科学誌「Cell Metabolism」のオンライン版に、1月17日付で発表された。
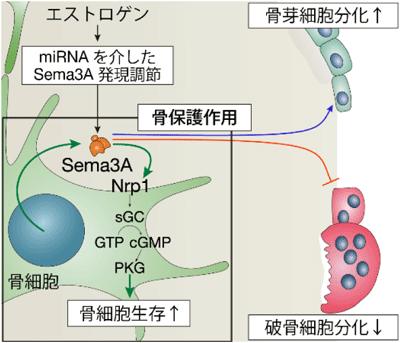
画像はリリースより
骨粗しょう症は、特に女性に多い病気として知られている。女性ホルモンの一種であるエストロゲンは、骨密度の維持に働いており、閉経に伴いエストロゲンの分泌が低下すると急激に骨密度が減るため、閉経は主たる骨粗しょう症の要因のひとつとなっている。しかし、エストロゲンが骨細胞を介して骨の細胞を調節・統合する仕組みは、これまで不明だった。
一方で、研究グループは以前、Semaphorin 3A(セマフォリン・スリー・エー:Sema3A)と呼ばれるタンパク質が、骨形成を促進し骨吸収を抑制することで骨を保護することを報告したが、そのタンパク質の発現制御機序や産生細胞などはよくわかっていなかった。
エストロゲンがSema3Aを制御
今回研究グループは、さまざまな細胞外因子で骨細胞を刺激し、Sema3Aの発現を上昇させるかどうかを調べた。結果、エストロゲンが濃度依存的にSema3Aの発現増強作用を持つことが判明。さらに、解析を進めたところ、エストロゲンによるSema3A発現増強作用はSema3aを標的とするマイクロRNAの発現抑制を介して行われていることが明らかになった。また、閉経後女性におけるSema3Aタンパク質の血中量を調べたところ、 閉経前女性の血中量よりも有意に低いことが判明したことから、実際に人間の体内でエストロゲンがSema3Aの遺伝子発現を調節している可能性が示された。
次に、研究グループは閉経後骨粗しょう症モデルとなるマウス(骨芽細胞系の細胞で特異的にSema3A遺伝子を欠失させ、卵巣を摘出したマウス)を作製。このモデルマウスにエストロゲンを投与しても、骨量が保たれなかったことから、骨芽細胞系細胞由来のSema3Aがエストロゲン依存的な骨量維持作用に重要な役割を担っていることが判明した。さらに、Sema3A発現量は、ヒトでもマウスでも加齢に伴って有意に低下することを発見したため、高齢のマウスにおいて骨芽細胞特異的、もしくは骨細胞特異的にSema3Aを欠損させたマウスの骨を解析した。結果、高齢マウスにおいては骨細胞が主にSema3Aを産生し、細胞自体や周囲の骨細胞に対して骨量維持作用を発揮している可能性が示された。
骨細胞が細胞生存シグナルの自己制御ループを形成
また、骨細胞でのみSema3Aが欠損した高齢マウスの骨では、骨細胞の数が著明に減少していることを発見。さらに詳細な解析を行った結果、骨細胞から産生されるSema3Aは、特に高齢において重要で、骨細胞自身に発現するSema3A受容体のNeuropilin-1(ニューロピリン・ワン:Nrp1)を介して、可溶型グアニル酸シクラーゼ(sGC)を活性化し、環状グアノシン一リン酸(cGMP)を介して細胞生存シグナルの自己制御ループを形成することで、骨量の維持に重要な役割を担っていることが明らかになった。閉経後骨粗しょう症のさらなる病態解明と、新たな分子機序の治療法開発への応用が期待される。
▼関連リンク
・東京医科歯科大学 プレスリリース



