さまざまな神経症状が現れる難治性の神経疾患
京都大学は9月13日、多発性硬化症の病態における新たな免疫細胞の役割とその作用機序の一端を明らかにしたと発表した。この研究は、同大学大学院薬学研究科の白川久志准教授、金子周司教授、筒井真人薬学部生(現・日本たばこ産業医薬事業部研究員)、平瀬僚薬学部生(現・マルホ株式会社探索研究部研究員)、宮村咲映薬学部生らの研究グループによるもの。研究成果は、国際学術誌「Journal of Neuroscience」に掲載された。
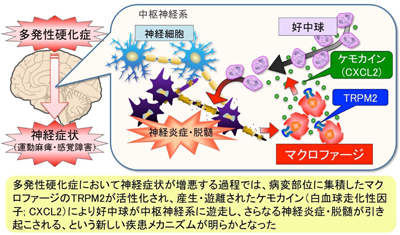
画像はリリースより
多発性硬化症は、運動麻痺や感覚障害、視力障害、排尿・排便機能障害、精神症状などのさまざまな神経症状が現れる難治性の神経疾患。詳細な原因はわかっていないが、神経細胞の軸索を覆っている髄鞘(ミエリン鞘)がリンパ球の攻撃により障害を受けることで発症する脱髄性の自己免疫疾患と考えられている。
TRPM2を抑制すると神経炎症の増悪が抑制
研究グループは、マウスを使って多発性硬化症の病態モデルを作成。神経炎症および脱髄の発生・増悪メカニズムを調べたところ、中枢神経系の神経炎症脱髄部位にマクロファージが集まっており、ケモカインのCXCL2を過剰に産生して好中球をその部位に大量に呼び寄せることで、さらなる神経炎症の増悪を引き起こしていることを見出した。また、そのマクロファージに発現する活性酸素種感受性のCa2+透過性陽イオンチャネルのTRPM2(トリップエム2)を抑制すると、その増悪が抑えられることも明らかにしたという。
今回の発見により、マクロファージ活性化に伴うケモカインCXCL2の産生・遊離、それに伴う好中球浸潤という、多発性硬化症の病態における新たな免疫細胞の役割とその作用機序の一端が明らかとなった。研究グループは、「活性酸素種感受性チャネルであるTRPM2の阻害や、マクロファージによる好中球浸潤の抑制が、多発性硬化症の新たな治療法の開発につながることが期待される」と述べている。
▼関連リンク
・京都大学 研究成果



