不明だった骨芽細胞に発現するRANKLの生理的な役割
東京大学医学部附属病院は9月6日、骨芽細胞に発現するRANKLが、破骨細胞から膜小胞の形で放出されるRANKを認識する受容体として機能しており、骨芽細胞分化の促進および骨形成の上昇に寄与していることを、RANKL遺伝子の点変異マウスを用いた解析などから明らかにしたと発表した。この研究は、同薬剤部の本間雅講師、池淵祐樹助教、鈴木洋史教授、東京医科歯科大学大学院医歯学総合研究科の青木和広教授らの研究グループによるもの。研究成果は「Nature」に掲載されている。
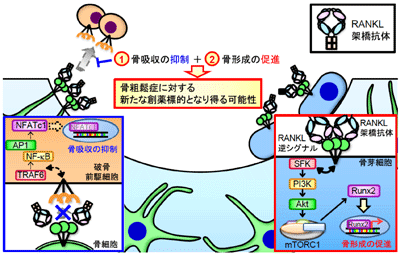
画像はリリースより
骨は、老朽化した部位が破骨細胞によって吸収除去され、続いて骨芽細胞による新しい骨の形成が生じて埋め戻される、という一連のサイクルを繰り返すことで骨量や骨質が維持されている。RANKLは骨芽細胞や、骨芽細胞から分化して形成される骨細胞に強く発現する分子で、ノックアウトマウスなどを用いた過去の解析から、破骨細胞の成熟を刺激して骨吸収を促進する中心的なシグナル入力分子であることが明らかにされている。また、生体内で破骨細胞に対してRANKLシグナルを入力している細胞は、従来は骨表面に局在している骨芽細胞であると想定されてきた。
しかし、骨細胞特異的なRANKLノックアウトマウスを用いた解析などから、生理的にRANKLシグナルの主要な供給源となっているのは、骨基中に分散してネットワークを形成している骨細胞であることが明らかにされたため、逆に骨芽細胞に発現するRANKLの生理的な役割に関しては不明瞭な状態となっていた。
RANKLの下流で転写因子「Runx2」が活性化
研究グループは、まず、破骨細胞からの分泌物を分析。破骨細胞の成熟段階にRANKの発現量が増大すると共に、RANKが含まれる膜小胞が盛んに分泌されることを確認した。この膜小胞を用いて骨芽細胞に対して刺激を加えたところ、骨芽細胞分化および骨形成が促進されることが判明した。RANKLノックアウトマウス由来の骨芽細胞では、この効果が認められないことから、破骨細胞由来の膜小胞の作用は骨芽細胞に発現するRANKLを介して生じていることも確認された。
次に、破骨細胞由来の膜小胞で刺激した骨芽細胞内で活性化しているシグナル伝達経路を解析したところ、RANKLの下流ではPI3K-Akt-mTORC1経路の活性化が生じ、最終的に骨芽細胞の分化を中心的に制御する転写因子であるRunx2の活性化が生じていることが明らかになった。また、骨芽細胞に発現するRANKLを起点とするRANKL逆シグナル経路は、生理的には骨吸収と骨形成のカップリングを媒介していることが示唆されたという。
骨粗しょう症の治療に用いられる骨吸収抑制剤は、強力に骨吸収を抑制する結果、カップリング因子の枯渇を引き起こし、骨形成も低下していく点が臨床上の課題となっている。今後、研究グループは、タンパク質としての産生量や安定性、生体内での半減期などをさらに改善した改変抗体の作出を目指して検討を進め、従来の薬剤の問題点を克服した、骨粗しょう症に対する新規治療薬の完成を目指すとしている。
▼関連リンク
・東京大学医学部附属病院 プレス発表



