不明な点が多い血球細胞以外の細胞の炎症メカニズム
京都大学iPS細胞研究所(CiRA)は9月3日、血管平滑筋細胞における新たな炎症発生のメカニズムを解明することに成功したと発表した。この研究は、元CiRA臨床応用研究部門の小野宏彰大学院生(現・九州大学医学部小児科特任助教)、CiRA同部門の齋藤潤准教授らの研究グループによるもの。研究成果は、国際炎症学会連合の機関誌「Inflammation Research」でオンライン公開されている。
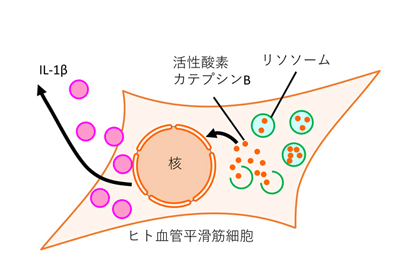
画像はリリースより
炎症反応メカニズムのうち最も重要なもののひとつに、NLRP3インフラマソームがある。NLRP3インフラマソームは、炎症性サイトカインであるインターロイキン(IL)-1βの分泌に関与するタンパク質複合体。主な炎症細胞である血球細胞からのIL-1βの分泌には、通常「準備シグナル」と「活性化シグナル」と呼ばれる2つの刺激が連続して伝えられることが必要とされるが、血球細胞以外の細胞により炎症が起きる場合、どのようにNLRP3インフラマソームが活性化しIL-1βが分泌されるかは、きっかけとなる細胞種によって異なる可能性があり、まだ詳細がわかっていないものも多くある。
血管平滑筋細胞は、血管壁の大部分を構成する重要な細胞で、刺激に応答して血管を広げたり縮めたりする機能を持っている。動脈硬化などの血管疾患においては、NLRP3インフラマソームによる慢性炎症が病気の進展に関与しており、血管平滑筋細胞にも炎症がおよぶことが示されている。一方、血管平滑筋細胞がNLRP3インフラマソームの関与する血管炎症でどのような役割を持っているのかは、まだ十分に解明されていない。そこで研究グループは、ヒト血管平滑筋細胞におけるNLRP3インフラマソームの活性化メカニズムの解明を目的として、今回の研究を実施した。
リソソーム膜の透過性亢進がNF-κB経路を活性化
免疫細胞において、リソソーム膜の透過性亢進は、NLRP3インフラマソームの重要な「活性化シグナル」であることが知られており、「準備シグナル」を受けて活性化した免疫細胞のリソソーム膜が壊れ、膜の内外を物質が通り抜けることができるようになると、NLRP3インフラマソームが活性化し、IL-1βが分泌される。一方、ヒト大動脈由来の血管平滑筋細胞では「準備シグナル」で刺激しなくても、リソソーム膜の透過性亢進のみでIL-1βが分泌されることが判明。この現象は、冠動脈や肺動脈由来の血管平滑筋細胞でも確認されたことから、ヒト血管平滑筋細胞に普遍的な現象であると考えられるという。
次に、リソソーム膜の透過性亢進がヒト血管平滑筋細胞からのIL-1β分泌を促すしくみを調査。リソソーム膜の透過性亢進は細胞死を誘導するが、ヒト血球細胞に比べてヒト血管平滑筋細胞では細胞死が起きにくいことが明らかになった。さらに、ヒト血管平滑筋細胞においては、リソソーム膜の透過性亢進がNF-κB経路といわれる炎症性経路を活性化し、「準備シグナル」としても働いていることがわかった。
さらに、リソソームに含まれる酵素や活性酸素がIL-1β分泌を促すかを調べたところ、酵素の一種であるカテプシンBや活性酸素を阻害すると、IL-1β分泌が抑制された。また、ヒト血管平滑筋細胞において、リソソーム膜透過性が亢進すると、カテプシンBの活性が「準備シグナル」を誘導し、活性酸素が「活性化シグナル」として働くことが判明したとしている。
近年、動脈硬化による血管変性のメカニズムとして、NLRP3インフラマソームの活性化による慢性血管炎症の関与が疑われている。今回の報告により、血管炎症の発生メカニズム解明がさらに進展することが期待される、と研究グループは述べている。
▼関連リンク
・京都大学iPS細胞研究所 ニュース




