年間1万人に1人が発症する網膜剥離
群馬大学は9月4日、世界で初めて網膜剥離時に視細胞死が起こる分子メカニズムを解明したと発表した。この研究は、同大大学院医学系研究科分子細胞生物学分野の柴崎貢志准教授が、同研究科眼科学分野の松本英孝講師らと共同で行ったもの。研究成果は米神経科学会誌「Journal of Neuroscience」にオンライン掲載された。
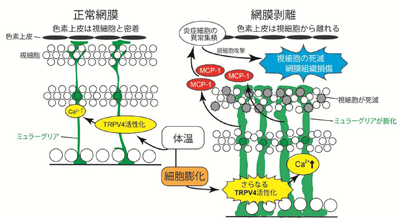
画像はリリースより
網膜剥離は年間1万人に1人が発症すると考えられている、失明を伴う重篤な疾患。網膜剥離では、色素上皮が視細胞の層から剥がれることが病態発症のはじまりで、色素上皮が剥がれると視細胞が次々に死滅し、最終的には失明につながる。しかし、なぜ網膜剥離になると視細胞が死んでしまうのか、そのメカニズムは不明だった。
TRPV4の阻害剤が視細胞死の治療に有効か
今回、研究グループは、実験動物のマウスに人工的に網膜剥離を起し、その病態がどのように進行して行くのかを分子レベル・細胞レベルで解析。その結果、網膜剥離になるとミュラーグリア細胞が著しく膨らむことが判明した。
ミュラーグリア細胞は、正常な網膜内では体温と細胞の伸び具合の両方を感知するセンサー「TRPV4」を用いて網膜内への栄養供給や老廃物除去を行っている。しかし、網膜剥離が起こった場合には、ミュラーグリア細胞が著しく膨らみ、TRPV4がその異常な膨らみ具合を感知し、異常に活性化するという。これにより、TRPV4から大量のカルシウムイオンが流入し、これが炎症性物質「MCP-1分子」の放出を引き起こすこと判明。この炎症性物質によって、本来は存在しないマクロファージが網膜付近へと引き寄せられ、最終的には大量のマクロファージによって視細胞が細胞死し、網膜組織が破壊されることが明らかになった。
また、研究グループは、ミュラーグリア細胞のみでTRPV4遺伝子を欠損させたマウスを作製し、この動物に網膜剥離を引き起こすと、視細胞死がほとんど起らないことを証明。正常マウスでは、網膜剥離時にTRPV4阻害薬を投与すれば、視細胞死を防ぐことができることを突き止めた。
今回の研究により、網膜剥離時にTRPV4の異常暴走を抑えることが視細胞死と網膜組織ダメージの進行を抑える有効な治療につながる可能性が示された。柴崎准教授は「網膜剥離の病態悪化を食い止めるためにはミュラーグリア細胞のTRPV4 センサーの働きをブロックすることがとても重要だと解明出来た意義は大きく、今後新たな治療法開発につながるのではないか」と述べている。
▼関連リンク
・群馬大学 プレスリリース




