ダイアモンド・ブラックファン貧血患者の中から発見
弘前大学は8月24日、ダイアモンド・ブラックファン貧血(DBA)と臨床的に診断された患者のなかに、がん抑制遺伝子「TP53」の活性化変異が原因で起こる新たな先天性骨髄不全症を発見したと発表した。この研究は、同大小児科学講座の土岐力講師、伊藤悦朗教授らと、京都大学医学部腫瘍生物学講座の吉田健一助教、小川誠司教授らとの共同研究によるもの。研究成果は、米学術雑誌「The American Journal of Human Genetics」にオンライン掲載された。
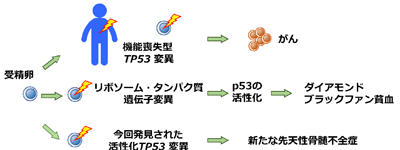
画像はリリースより
先天性骨髄不全症は、血液を作り出す細胞が先天的に障害され、赤血球や白血球などが減少してしまう病気の総称。その中に、赤血球の産生だけが障害され、新生児時から重い貧血に悩まされるDBAがある。DBAは、貧血の他に多指症などの奇形が約40%で認められることや、将来がんや白血病を発症しやすくなるといった特徴がある。
この病気には、がん抑制遺伝子TP53が重要な役割を果たしている可能性が以前から指摘されていた。TP53遺伝子の異常(変異)は、ヒトのがんで最も高い頻度で見られ、変異によりその遺伝子産物p53タンパク質が機能を失うためにがんが発生する。しかし、DBAではp53がどのような役割を果たしているか、詳細なところは明らかになっておらず、仮説のままとなっていた。
研究グループは、約10年かけて180例のDBA症例の原因遺伝子を検索。新たな原因遺伝子としてRPL27、RPS27、RPS15Aを発見してきた。しかし、日本ではまだ40%ほどの症例で原因遺伝子が分かっていない。
本来のP53遺伝子が作るタンパク質よりわずかに短く
これまで研究グループが調査した中に、典型的なDBAとは少し異なる2名の患者が含まれていたという。この患者らは、貧血に加え、低ガンマグロブリン血症、小頭症、高度の成長障害などの共通の臨床的特徴を持っていた。今回の研究では、両症例にはTP53に変異があることを発見し、DBAに類似した新しい先天性骨髄不全症であることを明らかにした。
がん細胞の中にみられる変異は、2万9,000種類以上が報告されており、これらの変異ではTP53の機能が失われる。一方、2症例でみつかった変異は、これまで報告されたものと異なっており、本来のTP53遺伝子が作るタンパク質よりわずかに短くなっていた。失われた部分は、p53で機能がよくわかっていない部分だったが、変異のあるp53の機能は活性化しており、これまでに見つかっていた変異とは性質が異なるものだったとしている。
DBAは、国内では年間に10例ほどしか発症しない希少疾患だが、今回10年に渡って全国の患者の変異検索をすることにより、その類縁疾患のひとつを発見することができた。今回の研究成果は、p53の活性化が骨髄不全症を引き起こすことを直接的に証明するものであると共に、TP53の機能について新たな知見を見出し、先天性骨髄不全症の新規治療法やがんの予防法の開発に結びつく可能性を提供するものだ、と研究グループは述べている。
▼関連リンク
・弘前大学 プレスリリース



