ドーパミン神経細胞の細胞死で発症するパーキンソン病
京都大学は8月31日、カルビンディン遺伝子を人為的に導入させ、ドーパミン細胞死を防御することに成功したと発表した。この研究は、同大霊長類研究所の井上謙一助教、高田昌彦教授らと東京都医学総合研究所、量子科学技術研究開発機構、生理学研究所の研究チームによるもの。この研究成果は、国際学術誌「Movement Disorders」にオンライン掲載された。
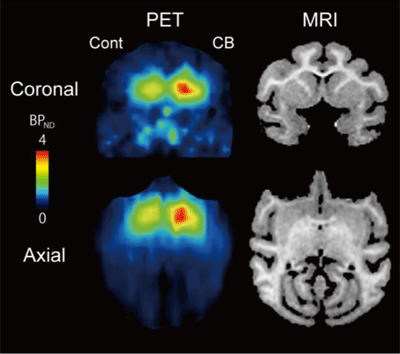
画像はリリースより
パーキンソン病が、中脳の黒質に分布するドーパミン神経細胞の細胞死によって発症することはよく知られている。黒質ドーパミン細胞には、カルシウム結合タンパク質のひとつであるカルビンディンを発現しているグループとそうでないグループとがあり、パーキンソン病では、カルビンディンを発現していないグループが発現しているグループに比べて細胞死を起こしやすいことが、これまでの研究によって明らかになっていた。
2つのウイルスベクターでカルビンディン遺伝子を導入
今回、研究グループは、正常ではカルビンディンを発現していないドーパミン細胞グループにカルビンディンを人為的に発現させることにより、ドーパミン細胞死を防御し、パーキンソン病の発症や進行を抑えることができると考え、パーキンソン病のサルモデルを用いて、この仮説を検証した。
この実験では、カルビンディンを人為的に発現させるために、カルビンディン遺伝子を搭載したウイルスベクターを作製。アデノウイルスとレンチウイルスに由来した2種類のベクターを利用した。アデノウイルスベクターは、黒質ドーパミン細胞が連絡している線条体に注入して逆行性に、レンチウイルスベクターは黒質に直接注入して、脳の片側のドーパミン細胞にカルビンディン遺伝子を導入した。
カルビンディンがドーパミン細胞に十分発現したと考えられる数週間後、ウイルスベクターを脳の片側だけに注入したサルに、静脈注射によりMPTPを全身投与した。その後の行動解析の結果、パーキンソン病に特徴的な無動寡動や筋固縮などの運動症状が、ウイルスベクターを注入した側に対応する、反対側の上下肢で軽減。また、陽電子放射断層撮影(PET)を用いて線条体におけるドーパミントランスポータ量を測定した結果、ウイルスベクターを注入した側で顕著に維持されていたことがわかったという。
行動解析終了後は、実験個体の安楽殺を行い、黒質と線条体を含む脳標本を免疫組織化学的に解析。その結果、正常ではカルビンディンを発現していない黒質緻密部腹側部のドーパミン細胞の多くにカルビンディンが発現していたこと、ウイルスバスターを注入した側ではドーパミン合成に関わるチロシン水酸化酵素の陽性細胞と要請細胞がそれぞれ黒質・線条体で優位に維持されていたこと、ウイルスベクターを注入していないコントロール側において、多数の黒質ドーパミン細胞でアルファシヌクレインの発現が増強していたことが明らかになった。
今回の研究成果から、パーキンソン病の発症や進行を抑える新たな治療法の開発に発展することが期待される一方、治療法の安全性を検証する必要がある。研究グループは、「ひとつのアプローチとして、iPS細胞を用いたパーキンソン病の再生医療において、移植するドーパミン産生細胞にあらかじめカルビンディン遺伝子を導入しておく、あるいは移植細胞としてカルビンディンを発現するドーパミン産生細胞を選択することが考えられる」と述べている。
▼関連リンク
・京都大学 研究成果




