ERKの活性を生きたマウスの腸上皮組織内で可視化
京都大学は7月4日、生体内での細胞増殖に関わるタンパク質「ERK」の活性を、生きたマウスの腸上皮組織内で可視化することに成功し、ERKの制御機構の一端を解明したことを発表した。この研究は、同大生命科学研究科の今城正道助教、松田道行教授、医学研究科の牟田優研修員らの研究グループによるもの。研究成果は「Nature Communications」に掲載されている。
生体内において、細胞は好き勝手に増殖するわけではなく、必要な時に必要な数だけ増えることが重要だ。多くの場合、細胞の増殖は、増殖因子が細胞表面の受容体に結合し、それを合図として細胞内でERKというタンパク質が活性化することで開始される。この機構の異常な活性化は発がんと関係しており、この機構を標的とした抗がん剤が開発されているが、これまでこのERKの活性を生体内でリアルタイムに観察することは技術的に困難だった。
腫瘍形成過程でEGFRの機能が増強、ERK活性の動態が変化
今回の研究では、ERKの活性を検出することができるセンサー分子(バイオセンサー)を全身で発現するようにした遺伝子改変マウスを使用。このマウスの組織を二光子励起顕微鏡で観察することで、生きたマウスの腸上皮細胞一つひとつでのERK活性の動きや変化をリアルタイムに観察(ライブイメージング)することができる研究手法を開発した。また、腸上皮細胞のオルガノイドを3次元で培養する技術を利用することで、薬剤投与や遺伝子機能の変化が ERK活性に与える影響も観察できるようになったという。
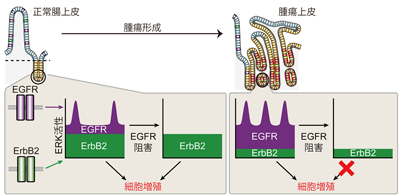
研究グループは、この手法を用いてマウスの腸上皮細胞を観察したところ、ERK活性には一定した活性と一過的なパルス状の活性という2つの活性の仕方があることを発見。画像処理や数理処理を行い、ERKの活性動態をくわしく解析すると、この2つの活性はEGFRとErbB2という2つの異なる増殖因子受容体によって、それぞれ制御されていることが判明した。さらに、腫瘍の形成過程ではERKのパルス状の活性が増加し、ERK活性動態にEGFRが寄与する割合が大きくなることを見出した。これらの研究成果は、大腸がん治療においてEGFR阻害薬が正常な腸上皮には重篤な副作用を示さず、大腸がんに選択的に効果を示すという実臨床における知見の生物学的背景を説明するものだという。
細胞増殖の適切な制御は、胚発生や成体組織における恒常性の維持、再生など、さまざまな生命現象の根幹を成しており、その異常はがんを始めとする多くの疾患と関係づけられている。今回の研究で使用されたERK活性の可視化技術を応用することで、これらの現象や疾患の理解が深まり、新たな治療法の開発に貢献すると期待されると研究グループは述べており、今後さまざまな生体分子の動態を一つひとつ解明することで、生命現象の新たなメカニズムを解明していくとしている。
▼関連リンク
・京都大学 研究成果



