E-SelectinをRUNX阻害剤で制御し、白血病細胞が骨髄に潜むことを抑制
京都大学は4月6日、骨髄微小環境(ニッチ)のひとつである血管内皮ニッチで重要な働きをするE-SelectinをRUNX阻害剤で制御することで、白血病細胞が骨髄に潜むことを抑制し、マウス白血病移植モデルにおいて生存期間を延長させることに成功したと発表した。この研究は、同大大学院医学研究科の上久保靖彦准教授、森田剣博士研究員、徳重智恵子修士課程学生、足立壮一教授、同大大学院理学研究科の杉山弘教授らの研究グループによるもの。研究成果は「Blood Advances」オンライン版に掲載された。
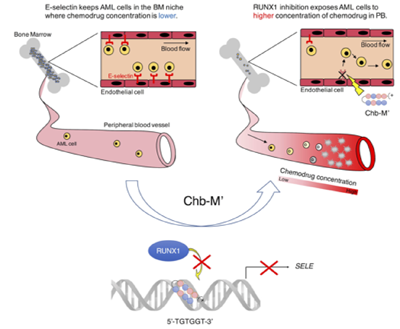
画像はリリースより
ニッチは、骨芽細胞ニッチと血管内皮ニッチに大きく分けられる。白血球と血管内皮細胞との接着に関与する分子セレクチンは、(E、L、P)-Selecinの3つが報告されているが、なかでもE-Selectinは血管内皮ニッチの重要な因子だ。急性骨髄性白血病細胞は、E-Selectinにより血管内皮ニッチに接着することで骨髄内に潜むことが知られている。
これまで研究グループは、RUNX1を白血病細胞で抑制することにより細胞増殖が強く抑制されることを実証してきたが、ニッチにおけるRUNXファミリー因子の働きは、ほとんど解明されていない。
白血病治療戦略にニッチ制御という新しい治療コンセプトを提示
研究グループは、まず、ヒトの血管内皮細胞株(HUVECs)において、研究グループが開発中のRUNX阻害剤(Chb-Mʼ)でRUNX1を特異的に抑制すると、E-Selectinの発現が最も強く抑制されることに注目。このとき、E-Selectinの転写を制御する領域に、RUNXファミリー因子の共通結合領域(コンセンサス配列TGTGGT)が存在すること、RUNX1がコンセンサス配列TGTGGTに結合し、E-Selectinの遺伝子発現を直接制御していることが判明したという。
次に、野生型マウスに2週間Chb-Mʼを投与し、骨髄のE-Selectinを強く抑制した後に、同系マウスの骨髄に、マウス急性骨髄性白血病細胞を移植。そのマウスより大腿骨と脾臓を採取し、その中の白血病細胞の比率を解析した。その結果、Chb-Mʼで前処置したマウスでは、大腿骨の白血病細胞比率が有意に減少したという。これは、大腿骨(骨髄ニッチ)に白血病細胞が潜むことが抑制されたことを示しているとしている。
また、免疫不全マウスに2週間RUNX阻害剤を投与し、ヒト難治性急性骨髄性白血病細胞を移植し、7日後生着を確認した後、Chb-Mʼで治療する実験を行った。その結果、ヒト白血病細胞を移植後無治療では、約40日でほぼマウスは白血病。Chb-MʼでE-Selectinを抑制後、ヒト白血病細胞を移植、その後無治療では、マウスの生存期間は延長し、約70日でほぼマウスは白血病死した。またChb-MʼでE-Selectinを抑制後、ヒト白血病細胞を移植、その後Chb-Mʼで治療した場合はさらにマウスの生存期間は延長し、約100日でほぼマウスは白血病死したという。
今回の研究によって、Chb-MʼなどによるRUNX阻害戦略は、白血病細胞に対するRUNX阻害剤の直接的抗がん作用だけではなく、ニッチを制御することで白血病細胞が骨髄内に潜むことを抑制するという非直接的な作用も、有効な治療戦略になる可能性が示唆されたとしている。これは、白血病治療戦略に、ニッチ制御という新しい治療コンセプトを提示するものだという。今後は、Chb-Mʼによるニッチ制御戦略の臨床応用が促進されることが期待されると研究グループは述べている。
▼関連リンク
・京都大学 研究成果



