Sipa1の欠乏で全く新しい細胞機能の調節機構を解除
京都大学は3月6日、慢性骨髄性白血病(CML)を引き起こす原因となる細胞を根絶する免疫メカニズムが、遺伝子「Sipa1」の欠乏によって発動する仕組みを解明したと発表した。この研究は、同大湊長博理事・副学長・プロボストらの研究グループによるもの。研究成果は「Nature Communications」に掲載されている。
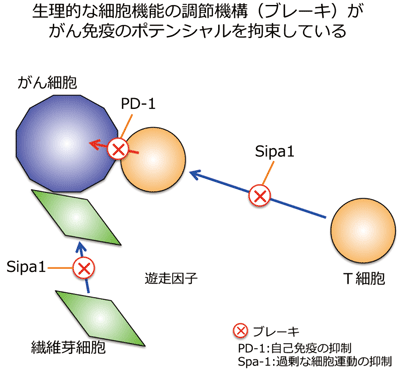
画像はリリースより
オプジーボなどのPD-1抗体による新しいがん免疫療法は、がん治療に画期的な進展をもたらした。これは免疫システムがもともと持っている調節(ブレーキ)機構を一旦解除することによって、がん細胞に対する潜在的な免疫反応を最大限効果的に発現させる。
今回、研究グループは、全く新しいタイプの細胞機能の調節機構を解除することによって、白血病細胞に対して非常に効果的な免疫反応が起こり、完全治癒にいたることを、動物モデルで発見したという。
薬剤耐性になった白血病に対しても有効
CMLは染色体の転座によってできるがん遺伝子(Bcr-Abl)を原因とするヒトの代表的な白血病。Bcr-Abl遺伝子を発現させた造血幹細胞を正常マウスに注射すると、CMLを発症して全例死亡する。しかし、遺伝子「Sipa1」を欠失させたマウスは、全く病気を発症せず全例生存したという。Sipa1は以前に研究グループが発見した細胞の「動き(移動)」を制御する分子だ。
正常マウスでは、免疫T細胞が白血病組織の近くにまでは来るが、その内部にまで入り込むことができない一方、Sipa1欠失マウスでは、免疫 T細胞が白血病組織の奥深くまで入り込んでいることがわかった。組織の繊維芽細胞が白血病細胞の近くに移動して細胞遊走因子であるケモカインを分泌、これを手がかりにエフェクターT細胞が白血病組織の内部に遊走し、直接白血病細胞を攻撃できると考えられるという。
がん免疫応答では、キラー細胞など免疫エフェクター細胞が実際の体内でがん組織にまで入り込み、がん細胞を有効に攻撃できるかどうかが重要な要素で、細胞の遊走能力はその成否に関わる。今回の発見によって、繊維芽細胞と免疫T細胞との連携による強力な白血病排除効果が発揮されうることが示された。現在ヒトのCMLに対しては、Bcr-Abl遺伝子の突然変異によってしばしば薬剤が効かなくなり再発にいたることが大きな問題になっている。しかし、今回発見されたがん免疫機構は、薬剤耐性になった白血病に対しても有効に働くことがわかっているという。今回の発見にもとづく創薬研究により、ヒトの白血病の根治にいたる新しい免疫療法が確立されることが期待される、と研究グループは述べている。
▼関連リンク
・京都大学 研究成果



