ALK/ROS1チロシンキナーゼ関連融合遺伝子を同定
名古屋大学は2月5日、若年性骨髄単球性白血病(JMML)の新たな原因遺伝子としてALK/ROS1チロシンキナーゼ関連融合遺伝子を発見し、この原因遺伝子を持つJMML患者にチロシンキナーゼ阻害薬を投与したところ、高い効果が確認されたと発表した。この研究は、同大大学院医学系研究科小児科学の高橋義行教授、村松秀城助教、村上典寛大学院生、小島勢二名誉教授らと、東京大学先端科学技術研究センターゲノムサイエンス分野の油谷浩幸教授、京都大学大学院医学研究科腫瘍生物学の小川誠司教授、国立がん研究センターの間野博行研究所長ら研究グループによるもの。研究成果は、米国血液学会発行の科学誌「Blood」に掲載されている。
乳幼児期におこる難治性の小児がんであるJMMLは、通常の化学療法の効果が低く、骨髄移植などの造血幹細胞移植が唯一の根治的治療法だが、造血幹細胞移植を行っても、いまだ約40%の患者が亡くなってしまう非常に予後不良な疾患。これまでの研究により、多くの症例ではRAS経路に関連した5つの遺伝子(PTPN11、NF1、NRAS、KRAS、CBL)が原因であることがわかっていたが、一部の症例では原因遺伝子が見つかっていなかった。
「高メチル化群」も非常に強力な予後不良因子と判明
研究グループは、150例のJMML患者で、次世代シーケンサーを用いて、全エキソーム解析などさまざまな網羅的な遺伝子解析を実施。その結果、RAS経路遺伝子に異常を認めない3人の患者から、ALK/ROS1チロシンキナーゼ関連融合遺伝子を発見したという。そのうち過去の2人の患者は、化学療法や骨髄移植といった標準的な治療に反応せず、発症後、早期に死亡しており、チロシンキナーゼ関連融合遺伝子を有するJMML患者の予後は非常に不良であると考えられた。また、研究期間中に発症した1人の患者では、診断後、早期にチロシンキナーゼ関連融合遺伝子(RANBP2-ALK)を確認。ALKチロシンキナーゼ阻害薬(クリゾチニブ)を用いた標的治療を行ったところ、投与開始後およそ1か月で腫瘍細胞がほぼ完全に消失し、完治することができたとしている。
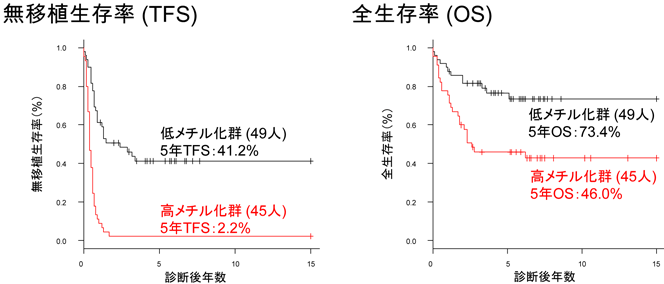
画像はリリースより
さらに、全メチル化解析の結果、遺伝子の制御に関わるDNAのメチル化が進んだ「高メチル化群」と進んでいない「低メチル化群」に、JMML患者を分類できると判明。高メチル化群に分類された患者の5年全生存率は46.0%と、低メチル化群(73.4%)と比較して明らかに予後不良だったという。また、高メチル化群が造血細胞移植を受けずに5年間生存できる可能性(5年無移植生存率)は2.2%しかなく、高メチル化群には造血細胞移植による治療が必須であることがわかった。この結果から、高メチル化群はこれまでに報告されているさまざまな予後不良因子と比較しても、非常に強力な予後不良因子であることが明らかになった。
今回、研究により発見されたALK/ROS1チロシンキナーゼ関連融合遺伝子は、すでに他のがんで標的治療が行われており、JMMLでも同様の標的治療の実用化が即時に可能と考えられる。また、研究グループは、「DNAメチル化に基づく層別化治療の開発により、JMMLの治療成績を改善することが期待される」と述べている。
▼関連リンク
・名古屋大学 プレスリリース




