同じ放射線量でも薬剤の種類などで殺傷能力が異なるBNCT
日本原子力研究開発機構(JAEA)は2月2日、ホウ素中性子捕捉療法(BNCT)の薬剤によるがん細胞殺傷効果の違いを理論的に予測する、新たな数理モデルを開発したと発表した。この研究は、JAEA原子力基礎工学研究センター放射線挙動解析研究グループの佐藤達彦研究主幹、京都大学原子炉実験所の増永慎一郎教授、筑波大学医学医療系の熊田博明准教授、電力中央研究所原子力技術研究所の浜田信行主任研究員の研究グループによるもの。研究成果は、英科学誌「Scientific Reports」に掲載されている。
BNCTは、ホウ素薬剤を投与した患者に中性子ビームを照射し、ホウ素と中性子の核反応で生じるα粒子やLiイオンによってがん細胞を殺傷する治療。体内でα粒子やLiイオンが飛べる距離は細胞1個分程度(~10μm)のため、がん細胞に薬剤を集中して取り込ませれば、正常細胞にあまり損傷を与えずにがん細胞のみ選択的に破壊することができるとして、がん細胞と正常細胞が混在している悪性度の高い脳腫瘍などで、とくに効果的だ。また、BNCTは同じ放射線量でも投与する薬剤の種類や濃度によってがん細胞殺傷能力が異なるが、その詳細な依存性やメカニズムはまだ解明されていなかった。
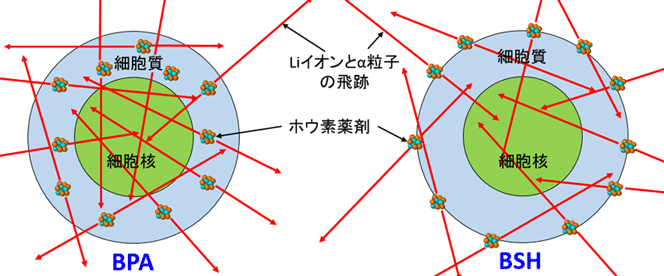 画像はリリースより
画像はリリースより薬剤の不均一な分布が治療効果の違いに
研究グループは、2種類のホウ素薬剤をさまざまな濃度で投与した担がんマウスに中性子を照射し、その治療効果を定量的に調べた。また、原子力機構を中心に開発した放射線挙動解析コードを用いた細胞レベルの放射線量解析によって、動物実験で示唆された薬剤による治療効果の違いが、薬剤が細胞内および細胞間で不均一に分布する効果に起因することを解明。この解析結果に基づき、薬剤濃度の不均一性を指標として治療効果を予測する新たな数理モデルを開発し、動物実験の結果を精度よく再現することに成功したという。
今回開発した数理モデルを応用すれば、新たなホウ素薬剤の治療効果の予測や患者個々人に合わせたより最適な放射線治療計画の提案が可能となるという。また、α線源内用療法など、他の放射線治療法への応用も期待される、と研究グループは述べている。
▼関連リンク
・日本原子力研究開発機構 プレスリリース



