分化に関わる転写因子を導入しても高い抵抗性を示す多能性幹細胞
慶應義塾大学は1月30日、ヒト多能性幹細胞であるES細胞やiPS細胞から、短期間かつ高い確率で骨格筋細胞に分化させる「細胞分化RNAカクテル」を開発することに成功したと発表した。この研究は、同大医学部坂口光洋記念講座(システム医学教室)の洪実教授らの研究グループによるもの。研究成果は「Scientific Reports」に掲載されている。
画像はリリースより
近年、転写因子をコードする合成RNAを試験管内で作製し、多能性幹細胞に導入する方法が開発され、ゲノム改変を伴わない簡便かつ安全な分化誘導系として広く普及しつつある。しかし、多能性幹細胞には、高い未分化維持性が存在し、分化に関わる転写因子を導入しても、迅速な分化が行われないという問題点があった。また、比較的分化誘導を起こしやすい線維芽細胞を骨格筋へと形質転換させるマスター転写因子「MYOD1」の導入による分化誘導にすら、多能性幹細胞は高い抵抗性を示すことが知られている。
分化誘導開始5日目に80%の細胞が骨格筋マーカーを発現
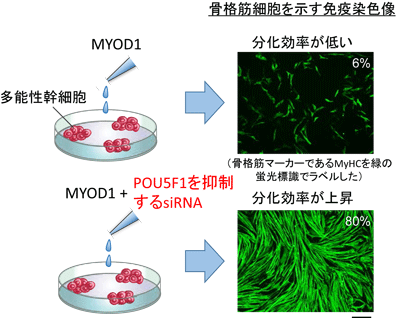
今回の研究では、まず従来通り筋細胞分化のマスター転写因子であるMYOD1の合成RNAを単独で多能性幹細胞に導入したところ、分化誘導がほとんど起こらないことを確認。分化誘導を阻害する遺伝子を特定するため免疫化学染色法によりMYOD1の導入された細胞に存在する複数の未分化関連因子の発現を調べたところ、未分化性を担う遺伝子POU5F1(OCT3/4)が残存していることがわかったという。
そこで、POU5F1を選択的に抑制するsiRNAとMYOD1の合成RNAを合わせた「細胞分化RNAカクテル」を作成し、多能性幹細胞に添加したところ、分化誘導開始から5日目に80%の細胞が骨格筋マーカーであるMyHCを発現していたという。また、この細胞はサルコメア構造や融合能を有する機能的な骨格筋細胞であることがわかったとしている。
さらに、網羅的な遺伝子発現解析を行った結果、POU5F1の抑制は骨格筋細胞分化に必須な成長因子の発現を促していることを発見。このことから、POU5F1の抑制は多能性幹細胞の未分化性を解除するだけでなく、多元的に分化誘導をサポートすることが示唆された。
今回の成果について、研究グループは、「骨格筋細胞の基礎研究のみならず、骨格筋の異常で起こるさまざまな病気の病態解明、治療薬の開発などに役立つことが期待される」と述べている。
▼関連リンク
・慶應義塾大学 プレスリリース






