ヒト正常大腸上皮細胞の動態を10か月以上観察
慶応義塾大学は2018年1月9日、ヒトの正常な大腸粘膜から培養した組織幹細胞をマウス腸管内へ移植してマウス生体内で生着させ、ヒト正常大腸上皮細胞動態を10か月以上の長期間にわたって観察することに世界で初めて成功したと発表した。この研究は、同大医学部内科学(消化器)教室の佐藤俊朗准教授らの研究グループによるもの。研究成果は「Cell Stem Cell」オンライン版に掲載されている。
日本には現在、16万人以上の潰瘍性大腸炎患者がおり、若年者を中心に近年増加の一途をたどっている。また、大腸がんによる死亡者数も年間約5万人と増加している。
正常な大腸上皮の組織には幹細胞が存在し、自分自身と同じ幹細胞を永続的に生み出す(自己複製)とともに、寿命が短く自己複製できない分化した細胞を次々と産み出すことで組織構造を作る。幹細胞だけが発現する遺伝子としてLGR5が考えられており、このLGR5を発現した腸管上皮幹細胞の機能の解明は、腸疾患の病態解明、根治に結びつくと期待されている。
ひとつのLGR5発現正常幹細胞が大腸上皮構造を半年以上かけて再構築
研究グループは2011年にヒトの腸管上皮幹細胞を体外で培養する技術(オルガノイド培養技術)を世界に先駆けて開発し、正常な幹細胞とがん幹細胞の研究を進めてきた。今回、研究グループは、オルガノイド培養技術にゲノム編集技術を応用することで、緑色蛍光タンパク質(GFP)を組み込んだ遺伝子改変オルガノイドを作製。このGFP発光するオルガノイドをマウスの腸管内に移植することで、生着成功の確認をマウス内視鏡システムを用いて行うことが可能となった。マウス大腸の上皮粘膜を剥離させる技術により、同部位に作成した遺伝子改変オルガノイドを10か月以上にわたり生着させ、ヒトの大腸上皮構造をマウスの腸管内で再構築することに成功した。
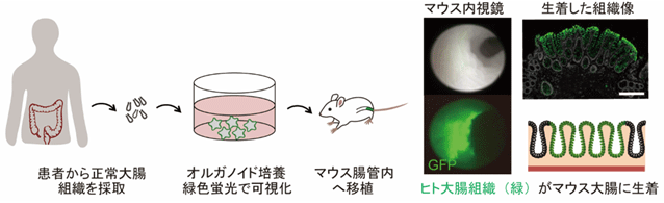
画像はリリースより
さらに、正常大腸幹細胞の機能的な解析を行うために、LGR5を発現する細胞をマークし、細胞系譜解析によりLGR5発現細胞の子孫細胞を異なる蛍光タンパク質で識別(可視化)するゲノム編集をオルガノイドに対して実施。この解析によって、たったひとつのLGR5発現正常幹細胞が、自分自身を産生するとともに、分化した子孫細胞を増やしながら大腸上皮構造を半年以上かけて再構築していく様子を経時的に捉えることができたという。
この結果から、これまでマウス細胞組織でしか証明されていなかった生体内での大腸幹細胞の存在を、ヒトの細胞組織において初めて実証した。炎症性腸疾患や大腸がんの根治を目指す上で必要な正常幹細胞機能の解明と、新規治療法開発への新たな糸口となる、と研究グループは述べている。
▼関連リンク
・慶応義塾大学 プレスリリース



