細胞のゲノム損傷の可能性などこれまでの方法には課題も
慶應義塾大学は12月22日、心筋梗塞モデルマウスの心臓に、細胞のゲノムを損傷することなく3つの心筋誘導遺伝子を導入して、梗塞巣の心臓線維芽細胞を効率よく短期間で、かつ直接的に心筋細胞へ転換して、心機能を改善することに成功したと発表した。この研究は、同大学医学部内科学(循環器)教室の家田真樹専任講師、宮本和享共同研究員らの研究グループによるもの。研究成果は、国際科学雑誌「Cell Stem Cell」のオンライン速報版で公開された。
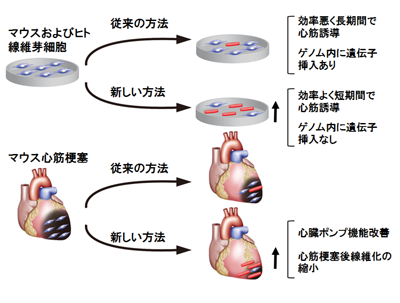
画像はリリースより
心筋梗塞、拡張型心筋症などの心臓病で心筋細胞が失われると、その部分は心臓内にある線維芽細胞の増殖、線維化により置き換えられ、心臓ポンプ機能が低下する。そのため、iPS細胞などの多能性幹細胞から作製する心筋細胞は、心臓病に対する細胞移植治療の細胞源として期待されている。しかし、iPS細胞等の幹細胞を用いる心臓再生治療の課題として、幹細胞混入に伴う腫瘍形成の可能性や、移植後の細胞の長期生着が困難であること、大量に心筋細胞を作成するコストが膨大であることなどの課題がある。現在、心臓病で一度線維化を起こし、正常な機能が失われた組織を元の心筋組織に戻す治療はない。
研究グループはこれまでに、細胞移植を必要としない新しい心筋再生法として、心臓に存在する心筋以外の心臓線維芽細胞に心筋誘導遺伝子を導入し、心筋を直接作製する研究を行っている。これまで、マウス生体内の心臓線維芽細胞にレトロウイルスベクターを用いた3つの心筋誘導遺伝子導入で、マウス生体内で直接的に心筋細胞を作製できることなどを報告している。しかし、これまでの方法では、心筋誘導の際にウイルスによって3つの遺伝子が組み込まれるために、細胞のゲノムを損傷する可能性があり、心筋誘導効率が低く心筋作製に長期間かかるという課題があった。
1週間で心筋再生が始まり、1か月後には心機能が改善
研究グループは今回、3つの心筋誘導遺伝子を同時に発現するセンダイウイルスベクター(心筋誘導センダイウイルスベクター)を、株式会社IDファーマと共同で開発。この心筋誘導センダイウイルスベクターを用いて、培養皿上で、効率よく短期間でマウスおよびヒト線維芽細胞から心筋細胞をゲノムの損傷なく、直接的に作製することに成功した。
心筋誘導センダイウイルスベクターをマウス心筋梗塞モデルの心臓に導入すると、1週間で心筋再生が始まり、1か月後には心機能が改善することを確認。不整脈や他臓器で心筋細胞が誘導されるなどの副作用は観察されなかったという。
これは細胞移植を必要としない新しい心筋再生法であり、心筋梗塞や拡張型心筋症をはじめとするさまざまな心臓疾患に対する再生医療への応用が期待される、と研究グループは述べている。
▼関連リンク
・慶應義塾大学 プレスリリース




