正常組織の放射線細胞死を防護し、がん細胞は防護しないp53制御剤
徳島大学は10月5日、正常組織の放射線耐性を高める放射線防護剤を開発したと発表した。この研究は、同大学大学院医歯薬学研究部医用理工学分野の森田明典教授らが、広島大学、東京理科大学、量子科学技術研究開発機構放射線医学総合研究所、東北大学、東京大学と共同で行ったものである。
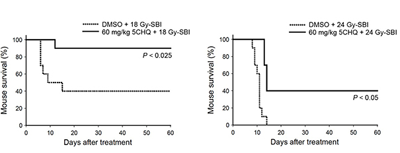
画像はリリースより
現在、継続的ながん医療を受けている国内の患者数は約150万人に上り、その内の約3割が放射線治療、約8割が化学療法の適応だ。これらの治療における副作用は、軽微なものも含めると発生率が高く、臨床的に深刻な正常組織障害が発生しない投与線量や投与量として処方するため、根治に至らない状況も生じる。そのため、これらの治療における副作用を軽減させる正常組織防護剤の開発が望まれている。
正常組織とがん組織を区別する大きな特徴として、半数近くのがん細胞では、がん抑制因子のp53に変異、あるいはウイルス由来因子による発現抑制や不活性化が見られ、p53機能が抑制されていることが挙げられる。p53制御剤は、正常なp53機能を示す正常組織の放射線細胞死を選択的に防護し、p53機能を喪失しているがん細胞は防護しないため、放射線被ばく事故での救命への応用だけでなく、放射線治療の投与線量の限界(耐容線量)を克服する副作用軽減剤としての応用が期待されている。
5CHQ活性がp53の放射線抵抗性機能を引き出す
今回研究グループは、p53分子内の亜鉛結合部位を標的とする8-キノリノール誘導体の合成、探索を進め、p53活性を制御するいくつかの放射線防護剤を発見。p53が有する標的遺伝子転写活性化能を調節する5-クロロ-8-キノリノール(5CHQ)に注目し、その放射線防護活性の詳細を明らかにしたという。
5CHQは、細胞周期を停止させることで放射線障害を受けた細胞の修復を促すp53標的遺伝子Cdkn1a(遺伝子産物p21)の転写を亢進させ、アポトーシスを促進するp53標的遺伝子Bbc3(遺伝子産物PUMA)の転写を抑制するp53転写の調節剤として機能することが判明。この特異な活性を有する5CHQは、腹部照射によるマウス腸死に著効を示す防護剤であることが明らかとなったという。この化合物の防護活性を示す線量減少率DRFは、骨髄死相当線量の全身照射試験で1.2、腸死相当線量の腹部照射試験で1.3と、新規の放射線防護剤として良好な値を示した。また、p53の遺伝子発現を抑制したノックダウン細胞や、ノックアウトマウスを用い、p53が正常に機能している細胞だけを防護することも実証したという。
p53の放射線抵抗性機能を引き出す5CHQの活性は、他に類を見ない化合物活性であり、放射線療法や化学療法を支援する新たな防護剤の創出が期待されるという。研究グループは今後、その作用機構の全容解明にさらに取り組むと共に、腫瘍モデル実験系で治療効果を向上させる働きがあるかどうかの検証を進めていくとしている。
▼関連リンク
・徳島大学 研究成果




