正常細胞と異なる代謝でエネルギーを産生するがん細胞
慶應義塾大学は8月29日、大腸がんの代謝が変化する仕組みを解明したと発表した。この研究は、同大先端生命科学研究所の曽我朋義教授、佐藤清敏特任助教、香川大学医学部消化器外科の鈴木康之教授、国立がん研究センターの谷内田真一ユニット長、愛知県がんセンター研究所の青木正博部長らの研究グループによるもの。研究成果は「米国科学アカデミー紀要(PNAS)」電子版に掲載されている。
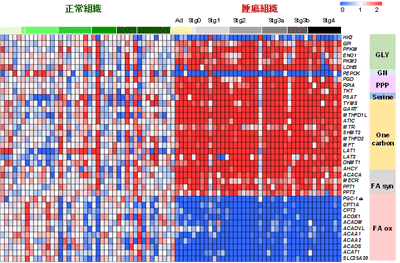
画像はリリースより
がん細胞は、正常細胞と異なる代謝を使って生存に必要なエネルギーを産生していることが知られている。この現象は、1920年代にドイツの生理学者オットー・ワールブルグによって発見された。
21世紀に入り、ワールブルグが発見した代謝以外にも、がんに特異的な代謝がいくつか見つかり、がん細胞はこれらの代謝を使って増殖に必要な生体分子をつくり出していることが判明。現在は、がんが示す代謝を阻害してがん細胞を死滅させようとする抗がん剤の開発が世界中で行われているが、がん細胞がどのようなメカニズムで代謝を変化させるかについては、よくわかっていなかった。
腫瘍形成の初期から代謝が変化
研究グループは、香川大学病院消化器外科において、合計275人の大腸がん患者からがん組織と正常組織を採取。その後、それぞれの組織に存在する数百の代謝物を、慶大先端生命研の曽我教授らが開発したキャピラリー電気泳動-質量分析計(CE-MS)によるメタボローム解析を用いて網羅的に測定した。
その結果、「大腸がんの代謝は良性腫瘍の段階から変化し、がんのステージによらないこと」、「がん遺伝子産物であるMYCタンパク質が215の代謝反応を介して大腸がんの代謝を変化させていること」を臨床検体で初めて証明。さらに、「MYCおよびMYCが制御している代謝酵素の抑制が大腸がん細胞の増殖を抑えること」を示し、「MYCが制御しているピリミジン代謝経路が、有望な大腸がんの治療法の標的になること」を示したという。
これらの研究成果について、曽我教授は、「AMED-CRESTでの多くの研究機関との共同研究によって、がんの謎であったがんが代謝をシフトするメカニズムを、臨床検体を用いてはじめて解き明かすことができた。この成果によって大腸がんの予防法や治療法の開発が進展すればうれしい」と述べている。
▼関連リンク
・慶應義塾大学 プレスリリース




