既存の細胞膜透過ペプチド、小腸吸収改善効果の小ささが問題に
熊本大学は8月21日、高分子であるバイオ医薬品の消化管吸収を促進させることが可能な新規小腸透過ペプチドを同定したと発表した。この研究は、同大大学院生命科学研究部(薬学系)微生物薬学分野の山口駿介大学院生、伊藤慎悟助教、大槻純男教授の研究グループによるもの。研究成果は「Journal of Controlled Release」に掲載されている。
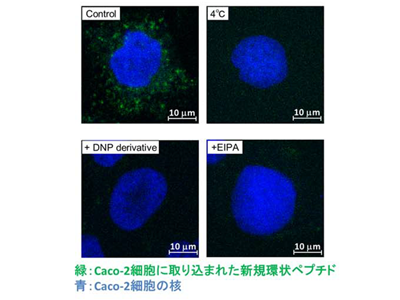
画像はリリースより
細胞膜透過ペプチドは、細胞膜を通り抜けて細胞内に内在化する能力をもつペプチド。これを細胞膜透過性が低いペプチドやタンパク質、核酸などに結合させることで細胞内への送達促進が可能になる。高分子医薬品の小腸吸収を促進させる方法として注目されているが、既存の細胞膜透過ペプチドをバイオ医薬品に結合させた場合、小腸吸収改善効果が小さいことが問題となっている。
バイオ医薬品の経口投与薬開発に期待
研究グループは、さまざまなアミノ酸配列の環状ペプチドを提示するファージ群の中から、ヒト小腸吸収モデルとして汎用されているCaco-2細胞層を透過するファージを集め、細胞を透過したファージが有するペプチドを解析。その結果、3種類の新規環状ペプチドを同定した。これらの環状ペプチドは、Caco-2細胞に加え、マウス小腸でもファージの小腸吸収を促進させたという。
既存の細胞膜透過ペプチドが消化管内で正に帯電するのに対し、最も透過能力の高い環状ペプチドは負に帯電するため、既知の細胞膜透過ペプチドとは異なるメカニズムによって、高い小腸上皮細胞透過能を発揮していると考えられる。この環状ペプチドの小腸吸収メカニズムを解析した結果、環状ペプチドは「マクロピノサイトーシス」という細胞外の巨大な物質を細胞に取り込む際に活用する仕組みを介して、細胞内へ移行していることが明らかになったという。
今回の研究成果は、分子量の大きなバイオ医薬品などに新規小腸透過性環状ペプチドを結合させることで、これまで注射剤として用いられてきた医薬品の経口投与を可能とするもの、と研究グループは述べている。
▼関連リンク
・熊本大学 プレスリリース






