細胞内に侵入してきた細菌を食べて殺す「ゼノファジー」
大阪大学は7月7日、血管の内皮細胞ではオートファジーによる細菌の除去ができないため、細胞内で細菌が増殖することを発見したと発表した。この研究は、同大のShiou-Ling Lu研究員らの研究グループによるもの。研究成果は、米科学誌「PLOS Pathogens」にオンライン公開されている。
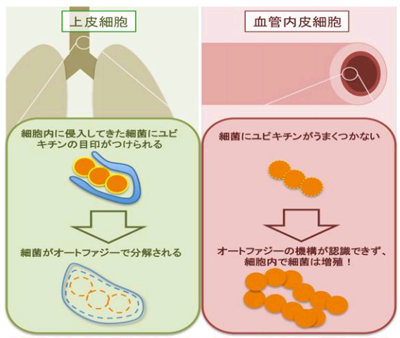
画像はリリースより
オートファジーは、栄養が足りない時にエネルギーなどを確保する経路として知られていたが、近年、損傷を受けたミトコンドリアなどさまざまな有害因子を選択的に分解し、細胞を助けていることがわかってきた。細胞内に侵入してきた細菌も例外ではなく、皮膚などの上皮細胞では、オートファジーにより細菌を食べて殺していることが明らかになっており、これをゼノファジーという。しかし、上皮細胞以外でのゼノファジーについては、これまでよくわかっていなかった。
細菌除去の潜在的な能力は備わっていることが判明
今回、研究グループは、細菌が血管内に入り込んで感染症が重篤化した時に、細菌の感染のターゲットとなる血管内皮細胞に注目。A群レンサ球菌などのさまざまな細菌を、ヒト培養細胞に感染させた。その結果、これらの細菌は上皮細胞内では増殖しなかったが、血管内皮細胞では増殖が止まらず、細胞死を引き起こしたという。電子顕微鏡で侵入した細菌の写真を撮影してみると、血管内の内皮細胞はオートファジーによる細菌の除去ができておらず、細胞内で細菌が増殖することが判明した。
細胞内に侵入した細菌には、タンパク質のユビキチンが付くことでオートファジーの食べる目印になるが、この標識が内皮細胞では上手く付いていなかった。そこで、細菌をあらかじめユビキチンでコーティングしてから血管内皮細胞に感染させたところ、細菌はオートファジーによって除去されたという。このことから、血管内皮細胞には、オートファジーにより細菌を除去するための潜在的な能力が備わっていることがわかった。今後、血管内皮細胞で細菌に特異的なオートファジーを誘導する方法を開発できれば、新たな感染症治療法につなげることが期待される、と研究グループは述べている。
▼関連リンク
・大阪大学 研究情報




