がん抑制遺伝子などの遺伝子転写を促進するヒストンのアセチル化修飾
科学技術振興機構(JST)は6月9日、ヒストンのアセチル化を選択的に行う人工化学触媒システム「SynCAcシステム」を開発、この触媒システムを用いてヌクレオソームをアセチル化することにより、遺伝子の転写を人工的に促進できる可能性が示唆されたと発表した。この研究は、東京大学大学院薬学系研究科の金井求教授らのグループによるもの。研究成果はCell Pressの「Chem」に掲載されている。
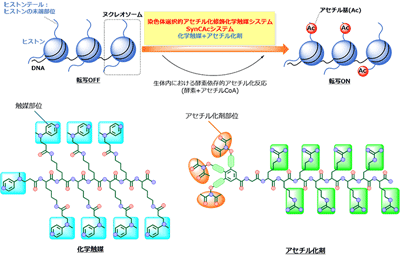
画像はリリースより
染色体の最小単位であるヒストンのアセチル化修飾は、がん抑制遺伝子などの遺伝子の転写を促進することが知られている。ある種のがん細胞のヒストンはアセチル化が抑制され、がん抑制遺伝子の転写も抑制された状態にある。研究グループは、生体内の酵素を介さずにヒストンのアセチル化修飾をすることができれば、がん細胞においてはがん抑制遺伝子を含む遺伝子の転写が活発になり、抗がん活性が発現して疾患の治療につながると考え、ヒストン選択的な化学触媒の開発に着手した。
酵素が失活・欠損している疾患で有効と期待される“触媒医療”
研究グループは、DNAが負の電荷性を帯びている性質を利用し、DNAに親和性をもつ分子として正の電荷性を持つ触媒とアセチル化剤を設計。これらを同時に用いる人工化学触媒システム“SynCAcシステム”(Synthetic Chromatin Acetylation)により、さまざまなタンパク質が混在する中でもヒストン選択的にアセチル化が進行することを発見した。さらに、この人工化学触媒システムによって導入されたアセチル化が、ヌクレオソームの性質を変化させること、染色体再構成因子という生体内に存在するタンパク質の存在下で転写を促進することも明らかにしたという。これの結果は、人工の化学触媒システムが生体内の酵素と同等の機能を示し得ることを示唆するものだ。
生体内に人工化学触媒システムを導入し、これが化学反応を促進することにより、生体に治療効果をもたらすという概念を研究グループは、“触媒医療”と呼んでいる。この概念から導かれる疾病治療は、とくに酵素が失活・欠損している疾患に対して、既存の手法よりも有効であるという。今回の研究成果は、基礎研究においては生体内反応の機能を解明するための有用な実験技術として、また臨床では疾患の新たな治療法の開発として、将来の医療の進歩に貢献することが期待される、と研究グループは述べている。
▼関連リンク
・科学技術振興機構 プレスリリース




