IDEに対して高い分解耐性を示すインスリンの作成目指す
東北大学は4月11日、ウシ膵臓由来の天然のインスリンに含まれるジスルフィド結合のひとつをジセレニド結合に置換した新規人工インスリン「セレノインスリン」の化学合成に成功したと発表した。この研究は、東海大学理学部化学科の荒井堅太講師および岩岡道夫教授、東北大学学際科学フロンティア研究所(多元物質科学研究所兼任)の奥村正樹助教、多元物質科学研究所の渡部聡研究員および同研究所(生命科学研究科および理学研究科化学専攻兼任)の稲葉謙次教授、大阪大学蛋白質研究所の北條裕信教授らの共同研究チームによるもの。同研究成果は、ドイツの国際化学誌「Angewandte Chemie International Edition」電子版に4月10日付けで掲載されている。
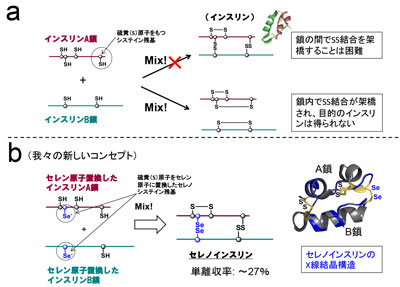
画像はリリースより
糖尿病患者にとって、インスリン製剤は命をつなぐ唯一の薬剤である一方、高頻度での皮下投与は肉体的・精神的な負担が大きい。創薬分野では、こうした患者の負担をできるだけ軽減しようと、長時間にわたって体内で循環・作用し、インスリンの基礎分泌を補助する新規持効型インスリン製剤の開発が大きな課題のひとつとなっている。
投与後に血流によって体内を循環したインスリンは、最終的に腎臓内でインスリン分解酵素(Insulin Degrading Enzyme; IDE)によって分解され尿として排出される。今回の研究では、このIDEに対して高い分解耐性を示すインスリンを人工的に作成することができれば、長時間体内を循環する新しいタイプの持効型インスリン製剤の開発につながると考えたという。
新規持効型インスリン製剤への応用に期待
インスリンは2本の異なるポリペプチド鎖のA鎖およびB鎖が、硫黄(S)原子同士のジスルフィド(SS)結合によって安定化されており、A鎖とB鎖からインスリンを得ようとしても鎖内のSS結合が優先して機能してしまうため、本来の目的のインスリンはほとんど得られない。そこで、研究チームは、Sよりもさらに反応性に富んだセレン(Se)原子に着目し、SをSeに置き換えたインスリンA鎖およびB鎖を用いれば、迅速に鎖間でジセレニド(SeSe)結合が形成されるため、両ペプチド鎖の会合反応を効率的に行えるのではないかと仮説を立てた。さらに、SeSe結合はSS結合よりも安定しており、インスリン分子に対して立体構造の“硬さ”と、それに起因するIDE分解耐性を同時に付与できるものと予想。このようなコンセプトのもと、まずはSe含有インスリンA鎖およびB鎖の化学合成に着手し、それらを得ることに成功した。さらに各ペプチド鎖を最適な条件下で混合し反応させることで、目的のセレノインスリンを最大27%の単離収率で得ることに成功したという。
次に、X線結晶構造解析によって、セレノインスリンの三次元立体構造を解析したところ、人工のセレノインスリンは天然インスリンと同様の立体構造を有していることが判明。また、インスリン同様の生理機能を保持していることも確認した。さらにIDEを用い、天然インスリンおよびセレノインスリンの分解実験を行ったところ、セレノインスリンは天然インスリンよりも分解速度が著しく遅いことが判明したという。以上の結果から、セレノインスリンは体内での薬効が長時間持続すると考えられ、新規持効型インスリン製剤としての応用が期待されるとしている。
▼関連リンク
・東北大学 プレスリリース






