糖脂質により修飾を受けたアンカータンパク「GPIHBP1」
群馬大学は4月6日、血管内皮細胞アンカータンパク「GPIHBP1」に対する自己抗体が原因で高トリグリセリド血症(高TG血症)をきたすという新たな脂質異常症のメカニズムを解明することに成功したと発表した。この研究は、同大大学院医学系研究科臨床検査医学・医学部附属病院検査部の村上正巳教授、中嶋克行協力研究員らの研究グループが、米カリフォルニア大学ロスアンゼルス校(UCLA)Stephen G. Young教授、東京医科歯科大学藍真澄教授らと共同で行ったもの。研究成果は「The New England Journal of Medicine」オンライン版に4月5日付けで掲載されている。
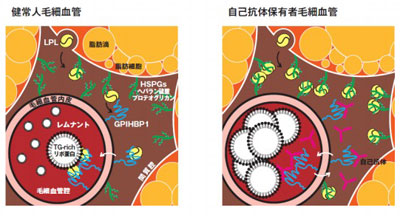
画像はリリースより
GPIHBP1(glycosylphosphatidylinositol anchored high density lipoprotein binding protein 1)は糖脂質により修飾を受けたアンカータンパクで、毛細血管内皮細胞膜上に存在し、TG-richリポタンパクの代謝に関与している。毛細血管の外側から血管の内腔にリポタンパクリパーゼ(LPL)を運ぶ役割を果たし、その遺伝子変異は高TG血症の原因となることが報告されている。GPIHBP1の役割についてはこれまで動物実験を中心に基礎的研究が行われてきたが、ヒトのGPIHBP1血中濃度測定法が確立されていなかったため、その臨床的意義の詳細については不明な点が多かった。
免疫抑制による新たな治療法が有効な可能性
研究グループは、GPIHBP1の酵素免疫測定(ELISA)法を開発し、ヒト血中濃度測定を可能に。この方法を用いて高TG血症(1000mg/dL以上)患者40例の血漿中GPIHBP1を測定したところ、健常人に比べて血中GPIHBP1濃度の低下傾向が認められた。さらに、これらの症例の血漿リコンビナントGPIHBP1を添加してその回収率を検討したところ、38例においては100%近くの回収率が認められたが、2例では10%以下の極めて低い回収率しか得られなかった。このことから、血漿中に自己抗体が存在する可能性を推測して詳細に検討した結果、これら2例はGPIHBP1対するIgG型の自己抗体を有することが明らかになったという。
今回の検討から高TG血症の全く新たな原因として、LPLが血管内皮細胞上で結合するアンカータンパクであるGPIHBP1に対する自己抗体の存在が判明。この自己抗体によりLPLの機能が阻害され、TG-richリポタンパクの代謝が機能せず、高濃度のカイロミクロンや超低比重リポタンパク(VLDL)が血中にうっ滞することが明らかとなった。今後研究グループは、これまで原因が不明だった国内外の著明な高TG血症の症例について、自己抗体によるものである否かを検討するとともに、より低濃度の高TG血症の場合における自己抗体の存在の可能性についても検討する予定。
また、高TG 血症の治療薬としてはこれまでフィブラート系の薬剤等が用いられていたが、自己抗体を有する患者には、免疫抑制による新たな治療法が有効な可能性がある。今後、脂質異常症の治療法として新たな薬剤の開発が期待される。
▼関連リンク
・群馬大学 プレスリリース




