初期化誘導遺伝子KLF4がiPS細胞誘導の効率を高める仕組みを解明
筑波大学は3月3日、人工多能性幹細胞(iPS細胞)誘導過程で、KLF4がTcl1遺伝子を誘導することによって細胞の代謝を変化させることを見出したと発表した。この研究は、同大学医学医療系の西村健助教、久武幸司教授らの研究グループによるもの。研究成果は国際幹細胞学会の機関誌「Stem Cell Reports」に3月2日付けで掲載されている。
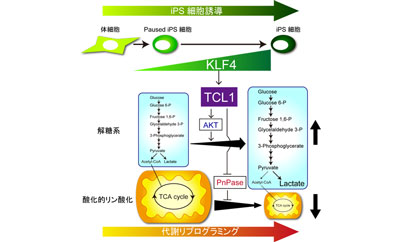
画像はリリースより
iPS細胞の誘導時には複雑な細胞機能の変化が起こるが、その変化の過程でどの遺伝子がどのように関与するかは、十分には解明されていない。iPS細胞の誘導過程で細胞機能を変化させる遺伝子とその作用機構を明らかにすれば、完全に初期化されたiPS細胞を効率良く誘導することが可能になると考えられる。
研究グループは、センダイウイルスベクターシステム(SeVdpベクター)を用いて、初期化誘導遺伝子 (KLF4、OCT4、SOX2、c-MYC)のひとつであるKLF4の発現量を操作すると、iPS細胞誘導が途中で停止した中間体(Paused iPS細胞)が作製できることを既に報告していた。
従来の方法よりも短期間でより多くの iPS細胞を誘導
今回研究グループは、Paused iPS細胞の初期化を再開するには、KLF4によってTcl1遺伝子が誘導されることが必要であり、この過程で細胞の代謝が変化することを明らかにした。また、同研究により、Tcl1遺伝子が細胞内でのエネルギー産生を体細胞型から多能性幹細胞型へと変換することによって、iPS細胞の誘導を促進することが明らかになった。Tcl1遺伝子は、iPS細胞誘導過程において、細胞によるブドウ糖の取り込みや乳酸産生を増加させるとともに、ミトコンドリアでの酸素消費を減少させるという。
さらに、Tcl1遺伝子を4つの初期化誘導遺伝子に加えてiPS細胞を誘導すると、従来の方法よりも短期間でより多くのiPS細胞が誘導された。これらの結果により、Tcl1遺伝子によって代謝変化(代謝リプログラミング)を加速すると、良質なiPS細胞を効率良く誘導出来る可能性が示唆された。
研究グループは、代謝リプログラミングによってどのようにして多能性が誘導されるのかは不明な点が残されているとし、今後はこの分子機構を明らかにし、さらに効率の良いiPS細胞誘導方法の確立に繋げることを目指したいとしている。また、Tcl1遺伝子以外にもPaused iPS細胞の多能性を向上させる候補遺伝子をいくつか見出しており、これらの遺伝子を介したiPS細胞誘導機構の解析も進めて行く予定だという。さらに同研究において、KLF4量のわずかな変化によって、Tcl1遺伝子の発現がどのように変化するかも明らかにできたことから、今後はTcl1以外の遺伝子でも同様な解析を進める予定だ。これらの解析によって、iPS細胞誘導機構の全容を明らかにするとともに、より一般的な、転写因子の量依存的な遺伝子発現調節機構についても重要な知見を明らかにしていきたいと、研究グループは述べている。
▼関連リンク
・筑波大学 お知らせ・情報




