注目される好塩基球によるMHCクラスII分子の産生と抗原提示能力
東京医科歯科大学は1月17日、細胞が別の細胞上にあるタンパク質を膜ごとかじり取る「トロゴサイト−シス」によって好塩基球が樹状細胞からアレルゲン情報を捕捉、T細胞に伝達することでアレルギー誘導型T細胞を生み出すという仕組みがあることを明らかにしたと発表した。この研究は、同大大学院医歯学総合研究科・免疫アレルギー学分野の烏山一教授(副学長・理事)の研究グループによるもの。研究成果は、国際科学誌「米国科学アカデミー紀要」オンライン版に1月16日付けで掲載されている。
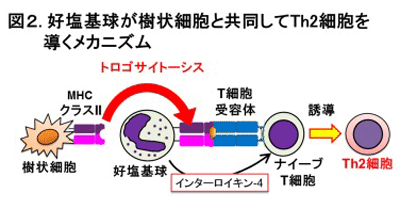
画像はリリースより
アトピー性皮膚炎や喘息に代表されるアレルギー疾患の患者数は年々増加しており、日本人の3割ほどが罹患しているといわれる。しかし、アレルギー疾患の根本的な治療法は確立されておらず、その病態解明が急がれる。アレルギー反応が引き起こされる過程では、T細胞(Tリンパ球)の一種であるTh2細胞が重要な働きをする。無垢なT細胞(ナイーブT細胞)は花粉などアレルゲンと出会うことでTh2細胞に変化(分化)。この際、抗原提示細胞と呼ばれる特殊な細胞が重要な役割を果たしており、MHCクラスII分子を介してアレルゲンをナイーブT細胞に手渡(抗原提示)する。これと同時にナイーブT細胞がもうひとつの刺激(インターロイキン4)を受けると、アレルギー誘導型のTh2細胞が誕生する。
これまで、樹状細胞が抗原提示細胞として機能し、樹状細胞とは異なる細胞がインターロイキン4を産生・供給し、分業することでTh2細胞が導かれるものと考えられていた。ところが2009年に、血中を流れる白血球のわずか0.5%を占めるに過ぎない希少な血球細胞「好塩基球」が、抗原提示とインターロイキン4産生の二役をひとりでこなしてTh2細胞を誘導することが報告された。これを機に、好塩基球によるMHCクラスII分子の産生とその抗原提示能力が注目されるようになったが、それを肯定する実験結果が出される一方で、否定する報告も出されるなど混沌とした状況が続いていた。
好塩基球が仲介役、樹状細胞からT細胞へとアレルゲン情報を伝達
研究グループは、好塩基球の細胞表面にMHCクラスII分子が検出できるにも関わらず、好塩基球自体はMHCクラスII分子を産生していないという現象を発見。生体内から取り出した好塩基球はMHCクラスII分子を細胞表面に出していなかったが、MHCクラスII分子を多く出している樹状細胞と一緒に培養すると、樹状細胞の表面上にあったMHCクラスIIが好塩基球の表面に移動することがわかったという。
詳細な解析から、この移動はトロゴサイトーシスと呼ばれるメカニズムによって起こることが判明。トロゴサイトーシスとは、2つの異なる細胞がくっつきあうことで、片方の細胞上にあったタンパク質が別の細胞上に移動する現象のことを言う。
さらに解析を進めると、好塩基球は、トロゴサイト−シスを巧みに利用してMHCクラスII分子だけでなくアレルゲン分子も一緒に樹状細胞から譲り受け、ナイーブT細胞に手渡すとともに自ら産生したインターロイキン4をナイーブT細胞に供給して、アレルギー誘導型のTh2細胞へと変身させることが判明したという。
今回の研究により、好塩基球がトロゴサイト−シスを駆使して樹状細胞からMHCクラスII分子を捕捉することによって抗原提示能を獲得することが明らかとなった。これにより先の研究で報告された好塩基球の抗原提示能に関する食い違いがなぜ起こるのかを説明できるようになった。同研究で解明された新たなメカニズムをさらに解析していくことで、アレルギー状態を改善する新規治療法の開発へ応用されることが期待されると、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース




