心臓の硬化により引き起こされる、左心室の拡張機能障害
生理学研究所は12月20日、心筋細胞膜に存在し、筋肉が持続的に伸展される刺激によって開閉するTRPC3チャネルが、コラーゲン線維の発現を誘導することを発見し、これが心臓組織の線維化を誘発し、心臓を硬くすることを発見したと発表した。この研究は、生理学研究所の西田基宏教授らが、北海道大学の渡辺雅彦教授、国立医薬品食品衛生研究所の佐藤陽治部長、九州大学の住本英樹教授、信州大学の桑原宏一郎教授、京都大学の森泰生教授、米国国立環境衛生科学研究所らと共同で行ったもの。研究結果は、「Scientific Reports」に12月19日付けで掲載されている。
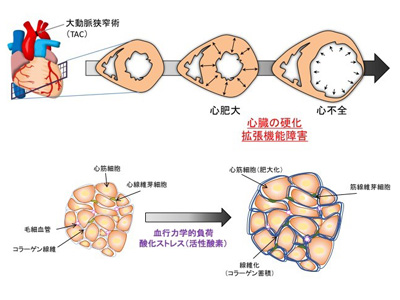
画像はリリースより
心不全患者の約50%近くは「拡張機能障害を伴う心不全」(HFpEF)。拡張機能障害の原因としては、活性酸素が過剰に産生されることによってコラーゲン線維が蓄積するなどといったことが指摘されていたが、高血圧などの力学的負荷によって心臓が活性酸素を生成する機構についてはよくわかっていなかった。
研究グループは今回、心筋細胞膜上に存在するCa2+透過型カチオンチャネル(TRPC3)を欠損させたマウスに大動脈狭窄を施し、高血圧と同様の圧負荷を与えたところ、圧負荷による心肥大は起こるものの、心臓の硬化と心機能不全がほぼ完全に抑制されることを見出した。通常、心不全マウスの心臓では酸化ストレスマーカーの発現量が顕著に増大する。ところが、TRPC3を欠損させたマウスの肥大した心臓では、酸化ストレスマーカーの発現はほとんど観察されなかったという。
心臓の硬化を防ぐ新たな治療薬の開発へ期待
そこで、酸化ストレスの原因となる活性酸素の生成酵素であるNADPHオキシダーゼという細胞膜タンパク質に着目したところ、TRPC3はNADPHオキシダーゼ2(Nox2)と相互作用し、Nox2タンパク質を安定化していることがわかった。
さらに、TRPC3チャネルは心筋細胞が機械的に伸展された際に活性化し、Nox2を特異的に活性化することも明らかにした。実際に、TRPC3とNox2の結合に必要なTRPC3チャネルを心筋細胞に発現させることで、TRPC3チャネルの活性化に依存した活性酸素の生成が抑制されることも確認された。これらの結果から、TRPC3チャネルはNox2の安定化と活性化を促進することで活性酸素シグナルを正に制御する役割を担うことが初めて明らかになったとしている。
今回の研究により、TRPC3チャネルが圧負荷誘発性の拡張機能障害を誘発する分子基盤がマウスレベルで明らかになった。今後、TRPC3チャネル活性あるいはTRPC3-Nox2相互作用を阻害する化合物の探索が、「心臓の硬化」を防ぐ新たな治療薬の開発へつながることが期待されると、研究グループは述べている。
▼関連リンク
・生理学研究所 プレスリリース




