成体の精巣内で精子に分化し、健常な子孫を産生
京都大学は12月7日、マウス多能性幹細胞(ES細胞)から、試験管内にて精子幹細胞様細胞およびその長期培養株Germline stem cell-like cells(GSCLCs)を誘導することに成功し、このGSCLCsが、生殖細胞を欠損する成体マウスの精巣中で精子に分化し、健常な子孫を生み出すことができたと発表した。この研究は、同大大学院医学研究科の斎藤通紀教授(兼科学技術振興機構(JST)ERATO斎藤全能性エピゲノムプロジェクト研究総括、京都大学物質-細胞統合システム拠点(iCeMS=アイセムス)主任研究者、京都大学iPS細胞研究所研究員)と、同研究科の石藏友紀子特定研究員らによるもの。同成果は、米科学誌「Cell Reports」オンライン速報版に12月6日付けで公開されている。
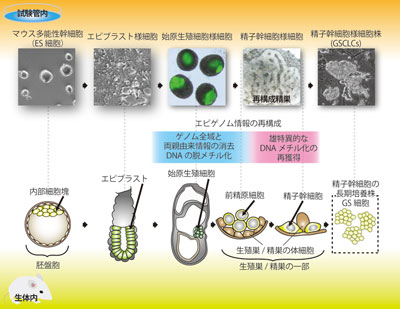
画像はリリースより
生殖細胞系列の分化過程や、生殖細胞に特徴的なDNAのメチル化を含むエピゲノム情報の再構成メカニズムを解明することは、不妊の原因究明や世代を経たエピゲノム情報の伝達メカニズムへの理解につながる。生殖細胞分化の重要な過程の多くは胎児成長の過程で行われるが、胎児の生殖細胞は、その細胞数の少なさやサイズが小さいことによる扱いづらさから解析が困難で、多能性幹細胞から生殖細胞系列の細胞を試験管内で誘導する試みが、四半世紀にわたって行われてきた。
近年、多能性幹細胞から精子や卵子の元となる始原生殖細胞を誘導する手法が確立され、それに続きオス、メス各々について配偶子分化過程の再現を目指す研究がなされてきた。オスについては、多能性幹細胞から始原生殖細胞を経て、精子の前段階の細胞である精子幹細胞を誘導することが目標のひとつとされてきた。
精子幹細胞におけるDNAのメチル化異常が精子形成不全につながることを発見
そこで研究グループは、マウス多能性幹細胞から誘導した始原生殖細胞様細胞を、胎仔(胎齢12.5日齢)の生殖巣体細胞とともに凝集させて作製した「再構成精巣」を培養することにより、始原生殖細胞様細胞から精子幹細胞に似た細胞を分化させ、これをGSCLCsとして試験管内で4か月以上長期培養することに成功。さらにこのGSCLCsを、生殖細胞欠損マウスの新生仔(生後7日齢)および成体(生後8週齢)の精巣に移植したところ、その一部が両精巣中で精子に分化し、健常な子孫を生み出すことができた。さらに、精子幹細胞形成過程におけるDNAのメチル化制御異常が、精子形成不全につながることを発見したという。
今回の研究で確立した培養システムと得られた知見は、男性不妊や、代謝疾患・精神疾患を含むエピゲノム異常症、遺伝病発症の原因究明に役立つことが期待される。また、同研究は、ヒト始原生殖細胞様細胞からヒト精子幹細胞様細胞を誘導する方法論の開発にも貢献する可能性があるという。
同研究グループは今後、より質の高い培養システムの確立や、世代を超えたエピゲノム情報継承メカニズムの解明に向けて研究を進めていきたいとしている。
▼関連リンク
・京都大学 研究成果




