移植したiPS細胞由来神経前駆細胞の脳内動態を生体脳で直接可視化
量子科学技術研究開発機構は11月9日、マウスの生体脳内に移植したiPS細胞由来神経前駆細胞が神経細胞に分化し、脳内で神経回路を形成したことをイメージングする新しい手法を開発したと発表した。この研究は、同機構放射線医学総合研究所脳機能イメージング研究部の季斌主任研究員、京都大学iPS細胞研究所(CiRA)らの研究グループによるもの。研究成果は「The Journal of Neuroscience」11月9日号に掲載されている。
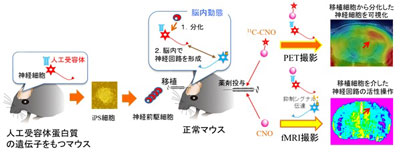
画像はリリースより
アルツハイマー病やパーキンソン病などの神経難病では、神経細胞死により認知機能障害や運動障害が起こるが、現在、根本的な治療法がなく、iPS細胞由来神経系細胞の移植による治療が次世代の治療法として期待されている。例えば、神経難病の一種であるパーキンソン病(PD)の治療研究では、PDモデルザルにおいてiPS細胞由来ドパミン神経前駆細胞の脳内移植による運動機能の改善が報告されているが、移植されたiPS細胞由来の神経細胞が、移植後の脳内で神経細胞に分化する過程や神経回路を形成するかどうかといった機能的な評価を、生体を傷つけずに実施する手段はなかった。
移植神経前駆細胞に由来する神経細胞の機能評価などに
同研究では、人工受容体とよばれる、生体内には存在しない低分子化合物(クロザピン-N-オキシド:CNO)が選択的に結合するタンパク質を目印に、移植細胞から分化した神経細胞を生体内で直接可視化する方法を開発。この方法では、CNOをポジトロン核種の11Cで標識したPET薬剤(11C-CNO)を合成。神経細胞に分化した場合にのみヒトムスカリン4人工受容体(hM4D)が発現する遺伝子改変マウス(hM4D-Tgマウス)から作製したiPS細胞を用い、作製した細胞を脳の海馬に移植した正常マウスに11C-CNOを投与してその脳をPETで撮像し、11C-CNOの集積を画像化することにより、生体脳で分化した神経細胞を直接可視化することが可能となった。
また、人工受容体にCNOを作用させて脳活動を抑制したマウスの脳をfMRIで撮像した結果、海馬内の移植した場所とは別の領域で脳血流の低下が確認されたという。これはiPS細胞由来神経細胞が他の領域の神経細胞との間に回路を形成したことを示唆するものだという。
今回開発された技術を用いることで、神経難病疾患モデル動物の脳に移植したiPS細胞由来神経前駆細胞が、いつ、どれだけ神経細胞に分化したかなど、脳内動態を生体で評価することが可能となった。移植した細胞の働きを、薬剤を用いて抑制または興奮させる操作を行った場合、細胞移植によって改善した症状がどのように変化するかを調べることで、移植した細胞の機能が症状改善にどの程度貢献しているかを知ることができるという。人工受容体を操作することにより移植細胞が治療効果を発揮するメカニズムの解明と、治療効果の予後予測による治療方法の最適化、治療方針の決定判断に大きく役立つことから、神経難病の再生医療を加速させると期待されると、同研究グループは述べている。




