韓国のKolon Life Science社とライセンス契約締結で
田辺三菱製薬株式会社は11月1日、韓国のKolon Life Science社との間で、変形性膝関節症の症状改善を目的とした細胞治療薬「Invossa(R)」に関するライセンス契約を締結したと発表した。同契約により、田辺三菱製薬は、日本におけるInvossaの独占的開発・販売権を取得する。
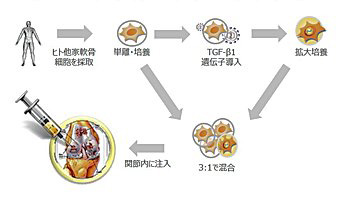
画像はリリースより
変形性膝関節症は、加齢とともに関節軟骨が弾力性を失い、物理的な摩擦が生じて軟骨がすり減ることを主な原因として発症する。主な症状は、膝の痛みや浮腫、可動域の制限など。現在の治療は疼痛緩和が中心であり、病態の進行抑制を適応とする治療薬はない。
Invossaは、KLS社の関連会社であるTissueGene,Inc.が創製した、ヒト他家軟骨細胞を用いた細胞治療薬。同種異系ドナーから採取した軟骨組織を供給源とし、単離・培養した軟骨細胞とTGF-β1遺伝子導入軟骨細胞を混合して関節腔内に注入する。TGF-β1遺伝子導入軟骨細胞が関節腔に混合注入した培養軟骨細胞の関節軟骨への生着を高めるとともに、これらの細胞が軟骨代謝異常を改善すると考えられる。変形性膝関節症の疼痛緩和効果が確認されており、さらに軟骨破壊進展を抑制することが期待されるとしている。
韓国で申請済み、米国でフェーズ3試験を準備中
KLS社が実施した韓国フェーズ3試験では、関節機能改善の指標であるIKDC(International Knee Documentation Committee)スコアおよび疼痛指標であるVAS(Visual Analog Scale)について、プラセボ群と比較しており、KLS社はこの結果をもって2016年7月に韓国の食品医薬品安全処(Ministry of Food and Drug Safety)に対し生物製剤許可申請を行った。米国でもTGI社がフェーズ2試験を終了し、フェーズ3試験を準備中。日本では、田辺三菱製薬が、変形性膝関節症を適応症として、軟骨破壊進展抑制作用の評価を含め、Invossaの開発を進める予定だ。
今回の契約締結により、田辺三菱製薬はKLS社に対して契約締結時一時金25億円を支払う。また、開発および販売マイルストン、さらに販売額に応じたランニングロイヤリティを支払う予定。なお、今回の件に関する業績への影響については織り込み済みとしている。
▼関連リンク
・田辺三菱製薬株式会社 ニュースリリース






