これまでにANGPTL2による生活習慣病やがんの促進明らかに
日本医療研究開発機構(AMED)は9月28日、老化した細胞やさまざまなストレスを受けた細胞から過剰に分泌されるタンパク質である「アンジオポエチン様タンパク質2(ANGPTL2)」が、心筋細胞内のカルシウム濃度調節やエネルギー産生機能を減弱させることで心筋の収縮力低下を引き起こし、心不全の発症・進展を促進することを明らかにしたと発表した。この研究は、熊本大学大学院生命科学研究部の尾池雄一教授らの研究グループによるもの。研究成果は英国のNature系科学誌「Nature Communications」オンライン版に9月28日付けで掲載されている。
画像はリリースより
心不全は、高血圧症や虚血性心疾患、心筋症などのさまざまな原因によって心臓のポンプ機能(心筋の収縮力や拡張力)が低下して、体に充分な血液を送り出せなくなった状態だが、重度の心不全患者においてはその5年生存率が約50~60%と低く、依然として非常に予後不良の病気である。心不全は健康長寿社会実現の大きな阻害要因になることからも、効果的な新規治療戦略の開発が望まれている。
研究グループはこれまでの研究で、ANGPTL2が、老化した細胞やさまざまなストレスを受けた細胞から過剰に分泌され、持続的な炎症(慢性炎症)を引き起こすことで動脈硬化性疾患、肥満症、糖尿病などの生活習慣病やがんの発症・進展を促進することを明らかにしている。
今回、研究グループは、加齢により老化した心筋細胞や高血圧などの圧負荷によるストレスを受けた心筋細胞、心不全患者の心筋細胞では、ANGPTL2の産生・分泌が増大していることを発見した。心筋細胞から過剰に分泌されたANGPTL2が心筋細胞自身に作用することで、心筋細胞内のカルシウム濃度調節やエネルギー産生といった心筋の収縮力を維持するうえで重要な機能を低下させ、心不全発症・進展を促進することを明らかにしたとしている。
ANGPTL2の産生を抑制する遺伝子治療法を開発
また、適度な運動は、心筋のポンプ機能促進により心不全発症に保護的作用をもたらすことがこれまで知られているが、今回、運動によって心筋細胞でのANGPTL2産生量が減少することを発見した。ANGPTL2を作り出せないようAngptl2遺伝子を欠損させた遺伝子改変マウス(Angptl2ノックアウトマウス)では、適度な運動を行った場合の心臓と同様に、心不全の発症が抑制され保護的作用をもたらすことがわかった。
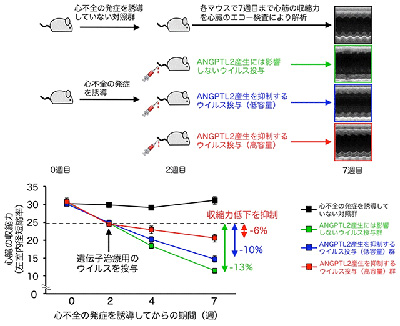
さらに、ANGPTL2の産生を減少させる作用をもった特殊なRNA分子(short hairpin RNA, shRNA)を産生できる病原性のないウイルス(アデノ随伴ウイルス)を遺伝子操作により作製し、このウイルスを心筋細胞に感染させることでANGPTL2の産生を抑制する遺伝子治療法を開発した。実際に、心不全モデルマウスでこの遺伝子治療を行ったところ、心筋細胞におけるANGPTL2産生量の増加が抑制され、心臓のポンプ機能低下が抑制されるなど心不全病態の進行を抑制することに成功した。
今回の新規遺伝子治療は、カルシウム濃度調節とエネルギー産生機能の両方を増進し、より効果的に心筋のポンプ機能を維持する治療法になることが期待される。さらに、今回、遺伝子治療を行っていないマウスに比べて遺伝子治療を行ったマウスの血液中のANGPTL2濃度が減少していたことから、血液中のANGPTL2濃度を測定しモニタリングすることで、遺伝子治療によるANGPTL2産生抑制効果を評価することも可能になると考えられる。
現在、心不全治療は対症療法が主だが、心筋細胞でのANGPTL2産生増加を抑制する遺伝子治療は、心機能低下のメカニズムそのものにアプローチする根本治療としての新規心不全治療戦略として期待できるだけでなく、健康長寿社会の実現にも貢献することが期待されると、研究グループは述べている。
▼関連リンク
・日本医療研究開発機構 お知らせ




