TレグがFoxP3遺伝子発現し、悪玉細胞制御か
京都大学は7月20日、同大学医学研究科の本庶佑客員教授らの研究グループが、PD-1分子が自己免疫疾患を抑制する機構の一端を明らかにしたと発表した。研究成果は、「米国科学アカデミー紀要」(Proceedings of the National Academy of Sciences of the United States of America)の電子版に7月7日付けで掲載されている。
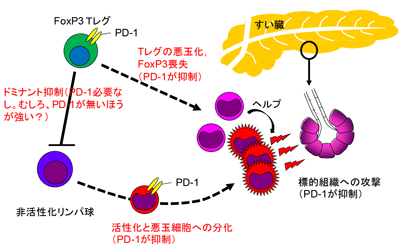
画像はリリースより
免疫系は、病原体やがん細胞をターゲットとして認識し攻撃、除去することによって、体を守る大切な仕組みだが、免疫系が自己をターゲットとみなし、攻撃してしまうと自己組織を破壊したり、深刻な自己免疫疾患を起こしたりすることがある。これを避けるために、過剰な免疫活性化を抑制するいくつもの仕組みが備わっている。
その中でも、PD-1分子と呼ばれる、活性化した免疫細胞に発現するレセプターは、ターゲットに対する免疫細胞の攻撃を弱めることが知られている。PD-1分子を欠損したマウスは、自己免疫疾患を自然発症するが、マウスの遺伝的背景により疾患の重症度、ターゲット組織が異なり、これを規定する第2、第3の因子があることは明白だった。PD-1と同様に、制御性T細胞(regulatory T cell:Tレグ)は、Forkhead Box P3(FoxP3)遺伝子を強く発現して、自己反応性の免疫細胞(悪玉細胞)を制御することによって、自己免疫疾患を抑制していると考えられている。
自己免疫疾患が起こる原因の究明に期待
研究グループは、TレグにPD-1が多く発現することから、Tレグの制御機能や恒常性をPD-1が調節すると考え、TレグにおいてPD-1の発現が直接必要なのか、あるいはPD-1とTレグは別々の抑制機構を発揮するのかを明らかにしようと試みた。
その結果、Tレグは、自己反応性の悪玉T細胞の活性化を間接的に抑制すること、一方でPD-1は、悪玉T細胞の分化や組織への攻撃を直接抑制すること、この両方の役割分担によって、自己組織に対する免疫系の暴走を抑えていることが明らかになった。また、PD-1の不全だけでは起こらない、致死的な自己免疫反応が、FoxP3の不完全な発現により重篤化することが示されたとしている。
近年注目される、PD-1をターゲットとしたがん治療法では、免疫増強の副作用として自己免疫疾患が問題となるが、今回の研究成果は一部の患者で自己免疫疾患が起こる原因の究明に役立つものと、研究グループは述べている。
▼関連リンク
・京都大学 研究成果




