マウスの腫瘍組織内の微小環境に注目して解析
理化学研究所は7月1日、マウスを用いて、現在開発しているがん治療製剤「人工アジュバントベクター細胞(aAVC)」に特徴的な抗がん作用機構を解明したと発表した。この研究は、理研統合生命医科学研究センター免疫細胞治療研究チームの藤井眞一郎チームリーダーらの研究チームによるもの。研究成果は、米国のがん学会科学雑誌「Cancer Research」に同日付けで掲載された。
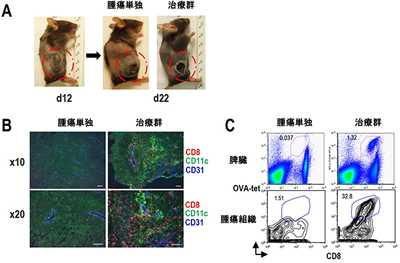
画像はリリースより
生体防御を担う免疫系には、先天的な免疫システムでさまざまな種類の抗原を対象に初期防衛を担う「自然免疫」と、抗体や多様な細胞性免疫応答によって特定の異物を認識し排除する「獲得免疫」があり、両者が協調して働いている。がん細胞は、その種類により自然免疫と獲得免疫に対する感受性が異なっているため、がんを完全に排除するには、自然免疫と獲得免疫の両者の活性化が必要となる。
研究チームは2009年にこの2つの免疫系を活性化させるaAVCを開発し、その有効性を解明する研究を進めてきていた。アジュバントは「免疫反応を増幅させる」こと、ベクターは「運び屋」を意味する。今回、aAVCによる治療効果について、マウスの腫瘍組織内の微小環境に注目して解析を実施した。
従来のがん免疫療法の2つの問題点克服
研究チームは、腫瘍が十分大きくなった時期にaAVCを静脈内投与したところ、腫瘍が壊死を起こし、縮小することがわかったとしている。このメカニズムを解明するために腫瘍組織を解析した結果、aAVC治療群のマウスでは腫瘍血管が接着分子を強発現し、その周囲に存在する樹状細胞がT細胞走化性CXCL10というケモカインを発現することで、活性化キラーT細胞を集めることを明らかにした。つまりaAVC療法によって、通常は腫瘍内に入り込むことができないキラーT細胞が、腫瘍内にアクセスできるようになることを突き止めたということになる。
さらに、研究チームはaAVCをマウスに投与し1年後に解析したところ、全身性に抗原特異的なメモリーキラーT細胞が維持され、再度同じ抗原に遭遇すると、このメモリーキラーT細胞が増幅して免疫を活性化させることがわかったとしている。これは、がんに対する記憶免疫が誘導でき、腫瘍局所のみならず転移および再発予防のために有効であることを示したことになる。
従来のがん免疫療法では腫瘍周囲の微小環境が改善できずにキラーT細胞ががん部位にたどり着けないことや抗がん効果が長続きしない問題点が指摘されてきたが、今回の発見は、aAVCが従来の問題点を克服できたことを意味する。今後治験に向け、新たな細胞製剤開発の研究を進めていきたいと、研究チームは述べている。
▼関連リンク
・理化学研究所 プレスリリース




