血管の成長・維持に必要なVEGFに着目
慶應義塾大学は6月21日、硝子体血管の可視化技術を確立し、血管の成長・維持に必要な血管内皮細胞成長因子(VEGF)に着目して研究を進めた結果、目の神経が出生後に、旺盛VEGFを取り込み消化することで、目の中のVEGF濃度を低下させ、硝子体血管を退縮させているというメカニズムを明らかにしたと発表した。
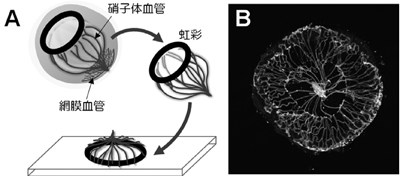
画像はリリースより
この研究は、同大医学部機能形態学講座の久保田義顕教授ら、同外科学(一般・消化器)教室の北川雄光教授との共同研究によるもの。研究成果は「The Journal of Experimental Medicine」オンライン版に6月20日付けで掲載されている。
ヒトの身体の血管ネットワークができあがる過程では、単に血管の枝分かれを増やし、広がらせるだけではなく、適宜不要となった部分を退縮させ、その時々のからだの成長に合わせた血管ネットワークへ作り変える必要がある。この「血管の取捨選択」で代表的なものが、胎児において使われていた血管が、出生後に必要となくなり退縮するという現象だ。この退縮がうまくいかなかった場合、さまざまな病態を引き起こすことが知られており、代表的なものに「第一次硝子体過形成遺残」がある。これは眼球における胎児特有の血管である硝子体血管が退縮しないことで発生する先天性の眼科疾患で、重度の場合、眼球内の組織傷害から重篤な視力障害を引き起こす。
特定の時期の特定の血管が自発的に退縮する現象を解明できれば、胎児血管退縮不全による先天性疾患の病態解明のみならず、がん血管を自発的に退縮させるがん治療の開発に応用することが可能。そのため、硝子体血管にフォーカスし、その退縮のメカニズムを解き明かそうとする基礎研究が、世界各国で盛んにおこなわれているが、そのメカニズムは解明されていなかった。
腫瘍を血行不全に陥らせる新規がん治療開拓の手掛かりに
その大きな理由のひとつとして、硝子体血管を明瞭に可視化し観察する技術がない、という点が挙げられる。研究グループが、硝子体血管の高精度な可視化技術の確立に取り組んだところ、硝子体血管が遠位部で付着する虹彩をテンプレートとして、機械的に一塊として網膜から分離し、染色作業をすることで、非常に明瞭に、かつオリジナルの構築を損傷することなく、硝子体血管全体を一視野のもと可視化することに成功。この技術を駆使し、体の中のあらゆる血管の成長・維持に必須である、VEGFに関わる種々の遺伝子改変マウスの硝子体血管を観察することで、研究を進めたという。
その結果、遺伝的に神経でのみVEGFを無効化させたマウスにおいて、硝子体血管の早期退縮が起こることを見出し、血管内皮細胞における2型VEGF受容体を欠失させると、同様に硝子体血管の退縮が促進されることを確認。これは硝子体血管が他の血管と同様、VEGF/VEGFR2シグナルに依存して生存していることを示す。
次に、網膜におけるVEGF発現について出生前後で定量を行ったが、着目すべき変化を認めなかった。一方で、VEGFR2に関しては出生直後の神経において著明な発現の増加を認めた。これを受けて、神経特異的VEGFR2ノックアウトマウスを作製したところ、眼球内のVEGFタンパク量が著明に増加しており、硝子体血管の退縮が著しく阻害されることを見出した。この表現型は神経でVEGFR2とVEGFの双方をノックアウトすることで打ち消された。これらの結果から、出生直後における硝子体血管の退縮は神経のVEGFR2を介した眼球内のVEGFの希釈を通じて、そのタイミングが精密にコントロールされていると考えられるとしている。
第一次硝子体過形成遺残について、これまで全く不明であった原因の一端が解明されたことにより、この疾患の新たな治療法の開発につながる期待が高まった。今回明らかにしたメカニズムは、硝子体血管にとどまらず、状況が整えば全身どこの血管であっても起こり得る現象であるため、発現を制御する技術が確立できれば、腫瘍の血管を自発的に退縮させ、腫瘍を血行不全に陥らせる新たながん治療の開拓の手掛かりとなることも期待されると、研究グループは述べている。
▼関連リンク
・慶應義塾大学 プレスリリース




