α位二置換非天然アミノ酸誘導体の効率的合成が可能に
九州大学は5月19日、ペプチド医薬品の原料として期待されているα位二置換非天然アミノ酸誘導体の不斉合成に有効な、末端アルキンの触媒的付加反応の反応機構解析および適応範囲の拡大に成功したと発表した。
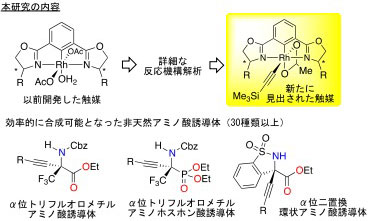
画像はリリースより
この研究は、同大大学院薬学研究院の大嶋孝志教授、森本浩之助教らの研究グループによるもの。研究成果は、国際科学誌「Journal of the American Chemical Society」オンライン版に、4月20日付けで発表された。
ヒトの体内で分泌される生理活性物質を根源とするペプチド医薬品は、副作用の少ない理想的な医薬品として期待されており、各種がんへの治療・応用が検討されている。しかし、構造が複雑で化学合成が難しいことや開発コストが高い等の要因があった。
反応性の向上・触媒量の低減化・適応範囲の拡大に成功
研究グループはこれまで、環境調和性に優れたα位二置換非天然アミノ酸合成に有効である、ロジウム触媒による末端アルキンの直接的付加反応を見出していた。今回、同反応の詳細な反応機構解析の結果、より高活性な新規触媒を見出し、反応性の向上・触媒量の低減化・適応範囲の拡大に成功したという。
これにより、種々のα位二置換非天然アミノ酸誘導体の効率的合成が可能となった。今回の研究結果は、同様の触媒反応の開発に新たな指針を与えるとともに、今後のペプチド医薬品の研究開発推進に期待が寄せられる。
▼関連リンク
・九州大学 プレスリリース






