がん治療、創傷治癒などに有効との報告があるプラズマ医療
東北大学は5月13日、大気圧ヘリウムプラズマの電子反応場を活用することによって、周辺大気を原料として液中に作りだした不安定な化学的活性種が、細胞膜の一過性受容器電位(TRP)チャネルを活性化し、生理的なカルシウムイオン(Ca2+)の細胞内流入を誘発することを突き止めたと発表した。この研究は、同大大学院工学研究科の佐々木渉太大学院生(日本学術振興会特別研究員)、神崎展准教授、金子俊郎教授ら研究グループによるもの。研究成果は、「Scientific Reports」のオンライン版に5月12日付けで掲載されている。
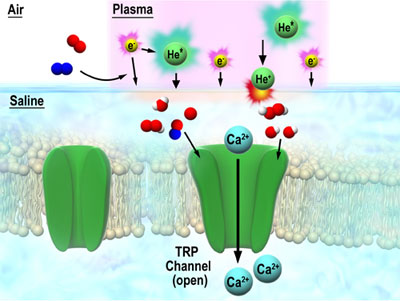
画像はリリースより
近年、手で触れられるほど低温な大気圧プラズマジェットを医療へと応用する「プラズマ医療」が盛んに研究されており、がん治療、創傷治癒、低侵襲止血、遺伝子導入等に有効であると報告されている。それらの多くの治療効果は、大気圧プラズマが生成する活性酸素種・窒素種に起因して得られることは知られているが、細胞が感知できる活性種の種類やその機構に関して不明な点が多く存在しており、プラズマ医療科学の発展やプラズマ医療機器開発に向けて、詳細な作用機序解明が望まれている。
過酸化水素以外の溶液中で失活する短寿命活性種がCa2+流入を誘発
今回の研究では、細胞を生きたまま観察するライブイメージング技術を用いることで、幅広い細胞応答に密接に関連する細胞内Ca2+濃度の変化を、プラズマ照射溶液を添加してからリアルタイム観測した。
プラズマを10秒照射した生理食塩水を細胞に滴下した結果、生理的な細胞内カルシウム上昇(あるいは振動)がみられた一方で、最終生成物の1つである過酸化水素(H2O2)では、このような現象はみられなかった。また、この細胞内Ca2+濃度上昇は、細胞外にCa2+が存在しない場合にはみられないこと、TRPチャネル阻害剤であるRuthenium Redと SKF96365の存在下で抑制されたことから、細胞外から細胞内へTRP チャネルを介した Ca2+流入が起因していることが分かるという。
さらに、プラズマを生理食塩水に照射してから、その溶液を細胞に添加するまでの時間(保持時間)の増加に伴い、細胞内Ca2+濃度上昇への効果が弱まったことから、溶液中において数分で失活する活性種が誘発していることが明らかとなった。これらの実験結果から、プラズマ照射に起因する過酸化水素以外の溶液中で失活する短寿命活性種が、TRP チャネルを介したCa2+流入を誘発していると結論付けられるという。
細胞内へのカルシウムの流入は、筋収縮、細胞分化、増殖、細胞死をはじめとしたさまざまな細胞応答のトリガーとなることが知られている。中でもTRPチャネルを介したカルシウム流入は多くの細胞において重要な役割を担っており、神経細胞においては、痛みや熱さ・冷たさ、味覚を感じるセンサーとして働いていると言われている。今回の研究成果は、既に報告されているプラズマ医療応用の作用機序解明に寄与するだけでなく、プラズマを用いた新たな生体機能制御を考える上での指針になると期待される。
▼関連リンク
・東北大学 プレスリリース




