脳室周囲に限局し、遊走能も低い神経幹細胞
東邦大学は4月13日、中枢神経系の自己再生を担う細胞である神経幹細胞の遊走能を外部から直接増強する機構を明らかにしたと発表した。この研究は、同大医学部生理学講座細胞生理学分野の浜之上誠准教授ら共同研究グループによるもの。研究成果は「Scientific Reports」オンライン版に4月12日付けで掲載されている。
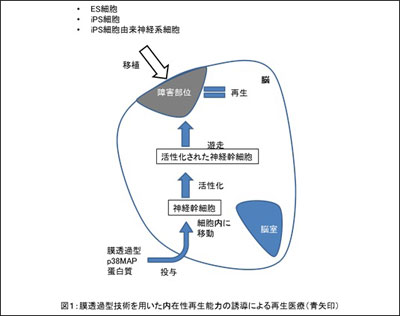
画像はリリースより
成人の中枢神経を構成する神経細胞は、分裂能力を喪失した細胞であることから、一度喪失した神経機能は回復しないと考えられていたが、現在ではヒトを含む中枢神経系にも内在性の再生機構といえる神経幹細胞が存在していることが知られている。しかし、この神経幹細胞は、その少数が成人の脳室周囲に限局し、かつ障害を受けた部位への遊走能も低いため、中枢神経系の低い再生能力の元凶の1つと考えられていた。
近年、この機能障害修復のために、生体外部で調整したiPS細胞から分化させた神経幹細胞や神経系細胞の移植、ウイルスベクターを介した遺伝子導入による再生医療が模索されているが、移植細胞のがん化や免疫原性・移植時期の制限、遺伝子導入に付随するウイルス毒性などの問題が指摘されている。
自己再生能力を活かした神経再生医療への応用に期待
研究グループは、マウスアダルト脳から調整した培養神経幹細胞の遊走能が、p38MAPキナーゼの特異的阻害剤により阻害されることを解明。p38MAPキナーゼが神経幹細胞に内在する遊走能担当因子であることを見出した。この結果から、細胞内のp38MAPキナーゼ蛋白質濃度を増加させることが神経幹細胞の遊走能を増強させると想定したという。
そこでp38MAPキナーゼ蛋白質に膜透過型ペプチドを付加した組み換え蛋白質を作成し、細胞外に添加した結果、膜透過型p38MAPキナーゼ蛋白質は速やかに細胞内に移行して、培養神経幹細胞の遊走能を著明に増強させることに成功。さらに、膜透過型p38MAPキナーゼ蛋白質は、神経幹細胞の生存や分化に影響を及ぼさない高い安全性を持つことも明らかになったという。
今回の研究により、生体外部からの細胞移植に頼らずとも、通常の投薬のように細胞外部から蛋白質を投与することで、ヒトに内在する再生能力を向上させ、機能再生を導く可能性があることが示された。また今回使用された膜透過型蛋白質技術について研究グループは、認知症や外傷などで細胞機能が障害されるような中枢神経疾患だけでなく、広範な全身疾患に対しての治療薬としての開発や応用が期待されると述べている。
▼関連リンク
・東邦大学 プレスリリース




