増殖因子とされる「Bone morphogenic proteinファミリー」の1つ
東北大学は3月31日、歯のエナメル質の厚さを制御するメカニズムを明らかにする研究結果を発表した。この研究は、同大学病院小児歯科の齋藤幹講師と、同大大学院歯学研究科小児発達歯科学分野の福本敏教授らのグループによるもの。研究成果は英科学雑誌「Scientific Reports」電子版に同日付で掲載されている。
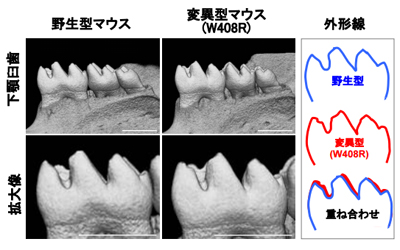
画像はリリースより
近年、iPS細胞等幹細胞を用いた臓器の再生研究が進んでいるが、ヒトの歯では、再生医療の実用化には臓器形成時間の短縮化が重要な課題となっており、増殖因子などを用いた歯胚形成の促進化が検討されている。Bone morphogenic protein(BMP)ファミリーは、骨を形成する蛋白質として同定された増殖因子の1つであり、現在までに15種類ほどが発見されている。その機能は骨や軟骨の形成だけではなく、胚細胞の発生や分化にも重要な役割を持っており、BMP2やBMP4は骨形成に関与するだけでなく、歯や毛髪等の形成にも関与するため、歯胚形成促進因子として注目されているという。
しかし、BMP2やBMP4だけでは歯のエナメル質形成には不十分であり、他の因子との併用が必要と考えられている。そこで研究グループは、14番目のBMPファミリーである「BMP14/Growth differentiation factor 5」(GDF5)が歯胚に発現することに着目。解析を実施した。
歯の大きさ調整や培養期間の短縮、再生治療への応用に期待
研究グループが歯の形成過程におけるGDF5の発現を調べたところ、間葉由来の歯周靭帯が形成される時期に発現を確認。さらにその発現を検討した結果、発現部位は歯周靭帯部だけではなく、エナメル芽細胞にも認められたという。GDF5が歯の上皮系細胞に発現していることはこれまで報告されておらず、この結果はGDF5がエナメル質形成に影響を与えている可能性を示唆するものだという。
そこで、GDF5の歯胚発生過程における役割を明らかにするため、GDF5の立体構造の解析を行い、受容体との結合部位を特定。この結合部位のうち、408番目のアミノ酸であるW(トリプトファン)がR(アルギニン)に変異した遺伝子組み換えマウスでは、関節の異常が見られる事が知られており、GDF5の408番目のアミノ酸変異は、GDF5の機能を阻害すると考えられてきた。しかし、GDF5に遺伝子異常を有するマウスの歯の形態をマイクロCTで解析したところ、エナメル質は肥厚しており、歯全体が一回り大きくなっていることが判明したという。
これを受け研究グループは、野生型の遺伝子配列であるUGGからAGGへと一塩基だけ遺伝子組み換えを行い、408番目のアミノ酸をWからRへ置換した変異型のGDF5蛋白を作成し、その機能を詳細に検討。同研究グループが以前樹立したラット歯原性上皮細胞株であるSF2細胞に野生型GDF5と変異型GDF5を遺伝子導入し、歯のエナメル質を誘導する蛋白であるアメロジェニンとアメロブラスチンの発現量を調べたところ、変異型 GDF5を導入した細胞でアメロジェニンとアメロブラスチンの発現量の顕著な増加が認められたという。BMP2がエナメル芽細胞のアメロジェニンやアメロブラスチンの発現を上昇させることは知られていたが、GDF5の変異は、その作用を更に増強し、エナメル質形成を促進されることが明らかになったとしている。
今回の研究より、軟骨や骨等の間葉系組織の形成に重要と言われていたGDF5が上皮でも発現しており、上皮由来エナメル芽細胞の分化調節を行なうことで、エナメル質形成に関与していることが新たに判明した。この結果により、歯のエナメル質形成メカニズムの解明や歯の再生における歯のサイズや作成時間短縮などの問題を解決する糸口になることが期待されるとしている。
▼関連リンク
・東北大学 プレスリリース




