プロスタグランジンE2が炎症を抑え、がんの増殖を促す
東京大学は3月29日、死を迎えたさまざまな細胞からプロスタグランジンE2(prostagalndin E2;PGE2)が放出されることを見いだし、死んだ細胞由来のPGE2が炎症・がんといった病態の進展に深く関与することを明らかにしたと発表した。
画像はリリースより
この研究は、同大大学院医学系研究科の半谷匠大学院生と同生産技術研究所の柳井秀元特任准教授らによるもの。研究成果は米国科学アカデミー紀要オンライン版に3月22日付けで掲載されている。
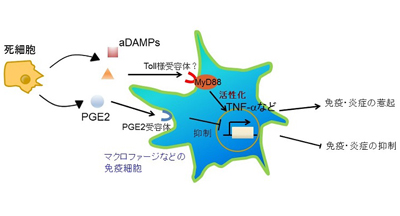
細胞が死を迎える際には、核酸やタンパク質が放出されて、炎症反応を起こすことが知られている。これらの分子はダメージ関連分子パターン(damage associated molecular patterns;DAMPs)と呼ばれ、炎症・免疫系を活性化し、自己免疫疾患や動脈硬化、がん、神経変性疾患など、炎症の関わるさまざまな病態に関わることがわかってきている。そのため、DAMPsはさまざまな疾患に対する治療標的として注目を浴びているが、DAMPsの中に炎症・免疫反応を抑える分子が存在するかどうかはわかっていなかった。
炎症性疾患やがんの病態進展メカニズムにつながる期待も
今回研究グループは、細胞が死ぬとPRE2が放出され、炎症・免疫系を抑制することを発見。実際に、細胞が死を迎える際にPGE2の放出を抑えた場合、炎症・免疫応答が増強されることも明らかになったという。さらに、肝障害を患ったマウスにおいてもPGE2の産生を抑制するとその症状が悪化し、死んだ細胞による炎症反応が増強されること、また、がん細胞においてもPGE2の産生を抑制すると、抗腫瘍免疫応答が増強され、がん細胞の増殖が抑えられることもわかったという。
ヒトの体内では、正常時でも1秒あたり10万個の細胞が死んでおり、また炎症性疾患やがんなどの疾患においても大量の細胞死が起こることがわかっている。これまで炎症・免疫系を引き起こす分子群として注目されてきたDAMPsの中に、炎症・免疫反応を抑える働きがあり、がんや炎症性疾患における役割が同研究で明らかとなった。同研究成果は、個体の恒常性の維持やこれらの疾患の病態進展のメカニズムに新たな視点を提供し、新たな治療法開発に向けた分子基盤の確立につながっていくものと期待が寄せられている。
▼関連リンク
・東京大学 UTokyo Reserch ニュース






