有効な標的が少なく、不均一であることが課題だった抗体医薬品
岡山大学は2月29日、同大学病院低侵襲治療センターの香川俊輔准教授、米国国立がん研究所(NCI)の小林久隆主任研究員らの研究グループが、遺伝子改変ウイルス製剤を用いて、標的抗原のないがんに人工的に標的抗原を発現させ、既存の抗体医薬品を用いた近赤外線光線免疫療法を応用する新たな治療法を開発し、ヒト胃がんを腹腔内に移植したマウスでその効果を実証したと発表した。この研究成果は、米科学雑誌「Molecular Cancer Therapeutics」電子版に2月1日付けで公開されている。
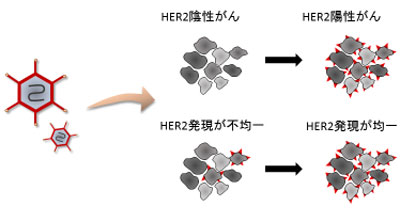
画像はリリースより
胃がんや乳がんでは、タンパク抗原「HER2」が細胞表面に出ており、がん細胞に特徴的であることから、HER2を標的とした抗体医薬品が開発され、臨床で抗腫瘍効果が得られている。しかし、そのような治療が適応できるのは、一部のHER2抗原を表出している細胞だけであり、結果的に抗HER2抗体は胃がん、乳がんのすべてを治療できないこと、その抗体薬も単独では、効果が弱いことが欠点だった。
一方で近年、近赤外線が当たると細胞を破壊する光感受性物質を抗体に結合させ、その抗体をがん細胞に運んで治療する光線免疫療法という新たな分子標的治療が開発され、抗体医薬品による抗腫瘍効果の向上が報告されていた。
有害作用が少ない光線免疫療法との組み合わせにも期待
今回、研究グループは、遺伝子改変ウイルス製剤により標的抗原タンパクであるHER2を積極的にがんに発現させることで、本来標的抗原を発現していないがん細胞に対しても、既存の抗HER2抗体薬をがん細胞に到達させて、近赤外線光線免疫療法を応用できることを証明した。
この研究では、標的抗原としてHER2がモデルとして用いられたが、ウイルスを用いた標的抗原の人工的発現は、これまで遺伝子治療で培われた技術と同様であり、理論上さまざまな種類のがん細胞に対して、抗HER2抗体にとどまらず、さまざまな抗原を標的とした抗体医薬品でも応用が可能と考えられるという。また有害作用が少ない近赤外線を用いる光線免疫療法との組み合わせは、新しい治療の選択肢として期待される。
同研究成果と遺伝子治療の研究開発で培われた技術を応用することで、標的抗原を強制的に発現できれば、標的のないがん細胞、不均一ながん細胞にも治療を施すことができ、がんを特異的に攻撃する分子標的治療を幅広い患者に届けることが可能になる。研究グル-プは今後、臨床応用を目指して、研究を進めていきたいとしている。
▼関連リンク
・岡山大学 プレスリリース






