生体リズムの異常伴う不眠症や生活習慣病の根本的是正に期待
京都大学は2月18日、同大学薬学研究科の土井雅夫准教授と岡村均教授らの研究グループが、生体リズム調整薬の開発に向け、体内時計を調節する新たなオーファンG蛋白質共役受容体(GPCR)の同定に成功したと発表した。研究成果は、英国科学誌「Nature Communications」誌で公開された。研究グループは、生体リズムの異常を伴う不眠症や生活習慣病の根本的な是正を目指した、新しいタイプの治療薬の開発につながる知見だと期待を寄せている。
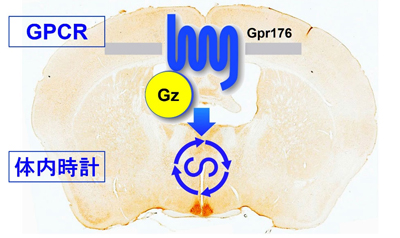
画像はリリースより
食事や血圧をはじめ、身体のほとんどの生理機能には24時間の規則正しいリズムがある。しかし、現在のような昼夜問わずの社会ではこのリズムが崩れることも多く、睡眠障害だけでなく、高血圧や糖尿病、発がんなどの生活習慣病につながることが示されている。
研究グループは、全身のリズムを統率する脳内の視交叉上核(SCN)に注目。親玉の仕組みがわかれば、生体リズム全体を操る方法を見つかる可能性が考えられる。しかし、生体リズムの機能障害が様々な疾患と関連することが知られている現在でも、SCNがなぜ強靱なリズムを発振できるのか、分子的な仕組みは明らかになっていない。
SCNに存在するオーファンGPCRを網羅的に検索
GPCRは薬理学上で最も重要、かつ効率のよいターゲットとして知られる分子群だが、いまだにその多くが機能未定のオーファン受容体である。研究グループは、SCNの機能を調律する新たなGPCRを同定するため、SCNに存在するオーファンGPCRを網羅的に検索した結果、SCNに強く発現し、遺伝子欠損によってマウス個体の活動リズムが変調するオーファン受容体Gpr176を同定した。
このオーファンGPCRは、これまでに知られる多くのGPCRとは異なり、Gzという特殊なG蛋白質を介して下流のcAMPシグナルを抑制する作用があり、SCN内においてGpr176が発するGzシグナルによって体内時計のスピードが調節されることがわかったとしている。
不規則な生活習慣によって生じる不眠症や高血圧症などの疾病を根本的に是正するためには、これまで開発されてこなかった脳内中枢時計機構に作用する新たな治療薬が効果を発揮する可能性があると考えられる。
Gpr176は末梢には発現せず中枢のSCNにのみに強く発現するという性質があるため、この分子を標的とすれば、生体時計の中枢に作用し末梢の臓器には影響を与えない創薬が可能となる。研究成果により、Gpr176に作用するリガンド物質やそれに対する拮抗薬を同定することができれば、中枢時計に作用する新たな医薬品の原体を得ることが可能できると期待されると研究グループは述べている。
▼関連リンク
・京都大学 研究成果




