線維芽細胞増殖因子加え、下垂体原基の形成効率向上も
科学技術振興機構(JST)は1月14日、名古屋大学大学院医学系研究科糖尿病・内分泌内科の須賀英隆助教、理化学研究所多細胞システム形成研究センター器官誘導研究チームの辻孝チームリーダーらの研究グループが、ヒト胚性幹細胞(ES細胞)を用い、下垂体前葉のホルモン産生細胞を分化誘導させる方法を確立したと発表した。
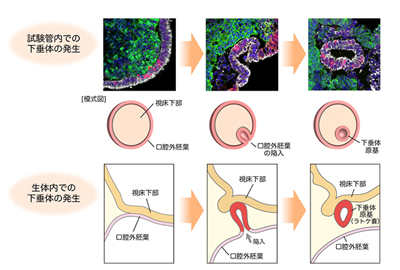
画像はリリースより
下垂体は、様々なホルモンを制御する司令塔ともいうべき中心的な働きをしており、成長・思春期・代謝・ストレス反応・妊娠・出産など、多岐にわたる生命現象をコントロールするのに重要な役割を担っている。そのため、下垂体ホルモン産生細胞の機能が低下すると、血圧低下や電解質異常、意識障害、成長障害、不妊など、様々な重い症状を引き起こす。現在、根治療法は存在せず、不足しているホルモンを投与する補充療法が行われているが、生涯にわたってホルモンを投与し続けなくてはならない問題点や、時々刻々と変動するホルモン必要量に対して現行の補充治療では十分には対応できない問題点がある。
下垂体は、生体内において口腔外胚葉と視床下部という2つの異なる組織が相互作用することによって形成されるが、研究グループは、ヘッジホッグシグナルを強める化合物(SAG)と骨形成タンパク質(BMP)をヒトES細胞に対して作用させることで、口腔外胚葉と視床下部を同時に試験管内で誘導することに成功、そこから下垂体原基が自己形成されることを示した。さらに、線維芽細胞増殖因子(FGF)を加えることで、下垂体原基の形成効率が向上することも明らかにした。
下垂体機能低下した患者の再生医療の可能性示す
この長期培養技術の向上を行った結果、ヒトES細胞由来の下垂体原基を成熟させ、ホルモン産生細胞に分化させることに成功した。下垂体前葉には、代表的な6種類のホルモン産生細胞があるが、その全てが分化誘導されることも確認。それらは生体内では分化の途中でいくつかの細胞系譜に分かれて生じることが分かっているが、今回の研究でもそれに即した誘導方法を確立したとしている。誘導されたホルモン産生細胞を電子顕微鏡で観察すると、内分泌細胞に特徴的な分泌顆粒が存在し、高い成熟度を得ていることが明らかとなった。
特に、副腎皮質刺激ホルモン(ACTH)細胞と成長ホルモン(GH)細胞については、試験管内でホルモン分泌刺激シグナルおよび抑制シグナル双方に正しく反応し、内分泌細胞としての機能を備えていることを示した。さらに、ヒトES細胞由来のACTH細胞を下垂体機能不全モデルマウスに移植し、血中ACTHやその下流で働く糖質コルチコイドが上昇すること、その結果、活動性や生存率が向上することも分かったとしている。
研究グループでは、下垂体の機能が低下した患者に対する再生医療の可能性を示しただけでなく、下垂体疾患の発症メカニズムの解明や新規薬剤の開発にも役立つと考えられると述べている。なお、研究成果は、英国科学誌「Nature Communications」に米国東部時間の1月14日付けで掲載された。
▼関連リンク
・科学技術振興機構 プレスリリース




