RISCが標的RNAを切断する過程を、1分子レベルで観察に成功
京都大学は7月8日、1分子イメージング技術を用いて、核酸タンパク質複合体「RNA-induced silencing complex」(RISC)が標的RNAを切断する過程を分子1個のレベルで観察することに、世界で初めて成功したと発表した。
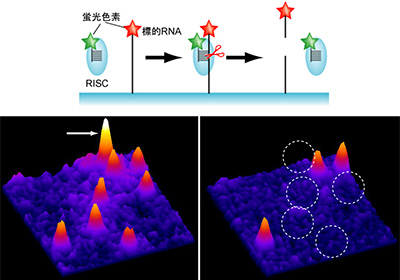
画像はリリースより
この研究は、同大の多田隈尚史物質-細胞統合システム拠点(iCeMS)特定研究員、東京大学新領域創成科学研究科の上田卓也教授、同分子細胞生物学研究所の泊幸秀教授らの研究チームによるもの。研究成果は、科学誌「Molecular Cell」に7月2日付けで掲載されている。
RNAiは、小さなRNAが標的とするメッセンジャーRNAの切断を引き起こし、特定のタンパク質の合成を抑えるという生命現象のこと。人工的に合成した小さなRNAやその前駆体を外部から細胞へ導入することで引き起こすことができるため、遺伝子のはたらきを調べる方法として生物学実験に幅広く利用されている。
小さなRNA1本鎖とアルゴノートと呼ばれるタンパク質からなる複合体であるRISCが、正しい標的を認識し切断することで、RNAiは引き起こされると言われている。これまでの研究から、RISCが「どのような」標的を切断するのかに関しては分かってきたものの、「どのように」切断するのかは詳しく調べる方法はなく、未解明な部分が多かったという。
RISCは標的を素早く、正確に切断する必要があるが、この2つは相反する性質である。これまでの生化学的、結晶構造学的知見から、RISCに内包する小さなRNA1本鎖が2つの部分(シード部分とその他部分)に分かれており、役割分担をしている事が示唆されていたが、直接的な証拠に欠けていたという。
複合体RISCが標的RNAを素早く正確に切る仕組みを解明
今回、研究グループはモデル生物であるショウジョウバエを用いて、RISCに取り込まれる小さなRNAに蛍光分子で目印をつけた。そこに1分子イメージング技術を用いることによって、RISCが標的を切断する過程を分子1個のレベルで、リアルタイムで観察することに成功。その結果、これまではとらえることができなかったRISCが標的を切断する詳細な過程が分子レベルで明らかになったという。
同研究では、リアルタイムに標的切断過程を観察することで、RISC はまずシード部分で素早く標的に結合し、その後、標的が正しいかどうかをその他部分で検証していること(校正機能)が直接的に観察されたという。一方で、標的切断後は2つの部分は明瞭な役割分担はなく、切断されて分断された標的は熱力学的安定性に基づいてランダムに放出されることが明らかになった。
これらの結果は、RISCが標的を切断する仕組みを解き明かす画期的な研究成果であるとともに、現在進められているRNAiを利用した次世代医薬品の開発など、RNAiのさらなる応用が加速することに期待が寄せられている。
▼関連リンク
・京都大学 研究成果




