近年国内でも増加傾向にあるメラノーマ
北海道大学は6月3日、同大大学院薬学研究院の松田正教授らのグループが、メラノーマがん細胞の転移を調節する細胞内タンパク質「Signal-transducing adaptor protein-2」(STAP-2)を同定したと発表した。
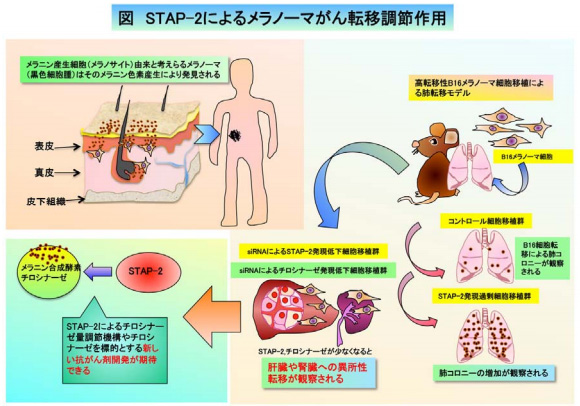
画像はリリースより
メラノーマは白人に多い皮膚がんだが、近年日本国内でも増加傾向にある。転移能の高さや転移発見後の5年生存率が低く、さらに化学療法や放射線治療が効きにくいことなどから悪性度の高いがんとして知られている。
発症にはさまざまな遺伝的、環境的要因の関与が指摘されており、メラノーマにおけるがん遺伝子として信号分子であるBRAFの変異が患者の半数に認められることからBRAFを標的とした分子標的薬が治療薬として使用されているが、その悪性度から新たな標的分子の同定と、より有効な抗がん剤の開発が待たれていた。
既存の治療薬との併用でメラノーマ治療の有力な武器となるか
今回、同グループは、シグナル伝達系において重要な信号調節分子であるSTAP-2タンパク質が、メラノーマがん細胞の転移においてどのように働くかを検討。高肺転移性マウスメラノーマB16がん細胞においてsiRNAにより内因性STAP-2発現を低下させたり、STAP-2を過剰発現させたメラノーマがん細胞を樹立し、STAP-2の細胞の形態変化や運動能、生存能への影響を解析した。
その結果、STAP-2発現はメラノーマがん細胞の形態、運動能や生存に影響しており、STAP-2を過剰に発現させたメラノーマB16がん細胞では肺転移の亢進が観察され、STAP-2 発現低下メラノーマB16がんでは肺転移が認められず、肝臓や腎臓など他の臓器への異所性転移が観察された。さらにSTAP-2発現はメラノーマがん細胞のメラニン合成酵素チロシナーゼ量を変化させることも明らかになったという。
これらの結果から、STAP-2はメラノーマ患者のための新しい抗がん剤開発の重要な標的であり、STAP-2やチロシナーゼを標的とした分子標的治療薬は既存の治療薬との併用により、メラノーマ治療の有力な武器になりえる可能性が示唆された。今後はメカニズムの詳細な解明に期待が寄せられる。
▼外部リンク
・北海道大学 プレスリリース




