国立がん研究センターのホームページ上で公開
国立がん研究センターは4月3日、英学術雑誌「Lancet Oncology」の3月号において、2016年度に導入予定の「患者申出療養(仮称)」の対象になると予想される抗がん剤(欧米先進国で承認され日本では未承認または適応外)の実態を報告。ホームページ上で「国内で薬事法上未承認・適応外となる医薬品・適応のリスト」(2015年1月末の時点の更新データ)を公開したと発表した。同リストにより抗がん剤におけるドラッグ・ラグの現状と、1か月にかかる薬剤費について把握することができる。
画像は同センターホームページより
患者申出療養(仮称)は、患者が希望すれば、迅速な審査で国内未承認の薬剤を使った医療を混合診療として認めるという制度(保険外併用療養費制度)。混合診療は一部の例外を除き原則禁止されているが、2014年6月24日に閣議決定された「日本再興戦略」改訂2014年の中でその創設が明記され、現在の通常国会で法案が審議される予定となっている。
薬剤費の大半は1か月当たり100万円以上
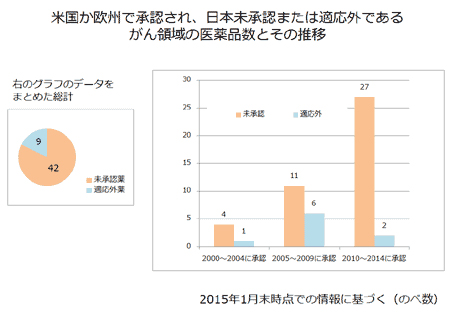
患者申出療養(仮称)の対象になると予想される抗がん剤は、2015年1月末時点で42剤。対象がん種は、主に血液がん、悪性黒色腫(メラノーマ)、前立腺がんであったという。これら抗がん剤の大半は、1か月当たり100万円を超える薬剤費が必要となる。患者申出療養(仮称)で適用される保険外併用療養費制度下では、薬剤費の多くは患者の負担となることが予想されており、制度が導入されても高額な薬剤費用を負担できる患者しか制度の恩恵を受けられない可能性が懸念されている。
▼外部リンク
・国立がん研究センター プレスリリース




