立体網膜の安定生産に向け、分化誘導技術を確立
理化学研究所は2月19日、理研多細胞システム形成研究センター器官発生研究チームの桑原篤客員研究員、立体組織形成研究ユニットの永樂元次ユニットリーダーらと、住友化学生物環境科学研究所の共同研究グループが、ヒトES細胞(胚性幹細胞)から、毛様体縁幹細胞ニッチを含む立体網膜(複合網膜組織)を作製することに成功したと発表した。この研究成果は、英国のオンライン科学雑誌「Nature Communications」に2月19日付で掲載されている。
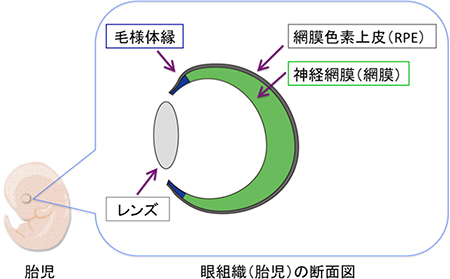
画像はプレスリリースより
毛様体縁は、胎児の網膜の端に存在する領域で、これまでに魚類や鳥類などで幹細胞を維持する特殊な構造(ニッチ)として働いていることが報告されていた。しかし、ヒトの毛様体縁の網膜発生における役割はほとんど明らかにされていない。これを解明するには、ヒト毛様体縁を含む立体的な網膜を安定的に作製する新たな技術が必要だ。
これまで理研では、「SFEBq法(無血清凝集浮遊培養法)」という分化誘導法を開発し、ES細胞やiPS細胞から、複雑な神経組織を作製してきた。網膜についても、マウスES細胞やヒトES細胞から立体網膜を作製している。今回、理研と住友化学の共同研究グループは、この技術をさらに改良して、新しい網膜分化誘導法の開発に挑んだという。
網膜色素変性を対象とした再生医療の実現化に向けて一歩前進
まず、ヒトES細胞をSFEBq法で分化させる条件を検討した結果、培養初期にBMP(骨形成因子)と呼ばれるシグナル作用物質を加えると、効率よく安定的に網膜組織へと分化誘導できることが分かったという。
次に、毛様体縁が胎児期の網膜と網膜色素上皮(RPE)の境目に形成されることに着目し、網膜とRPEが共存する「複合網膜組織(カブラ型網膜)」を目指した。さまざまな検討を行った結果、ヒトES細胞からBMP法で作製した網膜細胞をRPEに分化させ、その後、再び神経網膜を誘導する条件で培養して神経網膜に戻すという“揺り戻し法”を使うことで、神経網膜とRPEが共存した複合網膜組織の形成に成功したという。タミンの吸収変動を考慮した適切な薬物治療・薬用量設定に貢献するものと期待される。
そして、この複合網膜組織を分化60日目まで培養したところ、網膜とRPEの境界に、自己組織化により毛様体縁が形成されることが判明。毛様体縁を含む立体網膜を詳しく解析したところ、ヒト毛様体縁には幹細胞が存在し、この幹細胞が増殖する機能を発揮することで、網膜を試験管内で成長させることが分かったという。
研究グループは、この分化誘導技術を用いて生産した立体網膜を、網膜色素変性を対象とした再生医療に応用するための研究を進めていくとしている。
▼外部リンク
・理化学研究所 プレスリリース




