脂質代謝に重要なPPARαに着目、代謝物への変動を解析
京都大学は2月19日、生体内で生じる代謝変動の解析を行い、血中代謝物の生成機構と脂質異常症治療薬の新たな効き方の一端を明らかにしたと発表した。この研究成果は、同大学の高橋春弥農学研究科研究員、後藤剛同准教授、河田照雄同教授らと、かずさDNA研究所との共同研究によるもの。米科学雑誌「Journal of Lipid Research」誌に2月15日付で掲載されている。
画像はリリースより
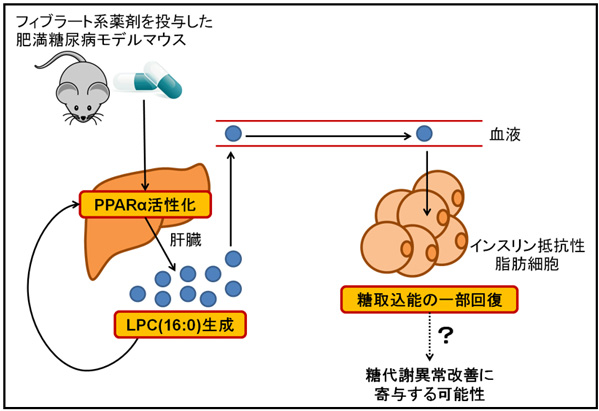
脂質異常症治療薬の一種であるフィブラート系薬剤は、主に脂質代謝に重要なPPARα(ペルオキシソーム増殖剤応答性受容体)の活性化を介してその薬効を発揮するといわれている。しかしながら、PPARαが活性化された後、最終的に生体内でどのような代謝変動が生じているのかについては未解明な部分が多かった。
LPC(16:0)の生合成機構が糖・脂質代謝異常を改善
研究グループは、最先端の分析技術「メタボローム解析」を駆使して、PPARαを活性化した際に、肥満・糖尿病モデルマウスの血中代謝物にどのような変動が生じるのか、その網羅的解析を行った。
その結果、脂質異常症治療薬投与によりPPARαを活性化させた際の血中代謝物変動の全体像を明らかにすると同時に、血糖値制御作用がある、リン脂質の一種である1-palmitoyl lysophosphatidylcholine (LPC(16:0))と呼ばれる代謝物の血中濃度が特徴的に変動することを見出した。また、この代謝物の生成機構の一端を明らかにしたという。
さらに、今回メタボローム解析で特定されたLPC(16:0)は、血糖値低下作用を有すること、および肥満・糖尿病進行時に血中濃度が低下することが知られている。そのため、同研究によって、フィブラート系薬剤がLPC(16:0)を介し、血糖値制御、すなわち糖代謝異常改善に寄与している可能性が新たに示唆されたという。
同研究グループは、LPC(16:0)の生合成機構が、糖・脂質代謝異常の予防あるいは改善に重要なターゲットとなり、新規の治療薬や機能性食品の創出につながることが期待されるとしている。
▼外部リンク
・京都大学 研究成果




