全生存期間について統計学的な有意差、改善見られず
武田薬品工業株式会社は6月19日、前立腺がん治療薬「TAK-700(一般名:orteronel)」の開発中止を発表した。
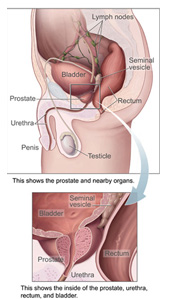
画像はwikiメディアより引用
この決定は、国際共同臨床第3相試験であるELM-PC4、ELM-PC5において、主要評価項目の1つである全生存期間について統計学的な有意差、改善が見られなかったことによるもの。
試験結果を精査・検討した結果、他に前立腺がんに対しては治療オプションが存在することも考慮し、同社は自主的にorteronelの開発中止を決定したという。
プレドニゾンと比較
ELM-PC4は化学療法を受けていない転移性・去勢抵抗性前立腺がん患者を対象に、ELM-PC5は化学療法実施中あるいは実施後の転移性・去勢抵抗性前立腺がん患者を対象に実施されたもの。プレドニゾンとorteronel併用群と、プレドニゾンとプラセボ併用群の比較が行われた。
どちらの試験においても、もう1つの主要評価項目である画像上での無憎悪生存期間については統計学的に有意なリスク減少、改善が見られた。また、安全性にも問題はなかったとしている。
プレスリリースでは
前立腺がんをはじめ、がん領域において革新的な治療薬を患者さんにお届けできるよう、引き続き研究開発に取り組んでまいります。(武田薬品工業株式会社 プレスリリースより引用)
と述べられている。(小林 周)
▼外部リンク
・武田薬品工業株式会社 プレスリリース




